サンバイオ(4592) 特別号 原点回帰の背景と意義
 森 敬太 社長 |
サンバイオ株式会社(4592) |
 |
企業情報
|
市場 |
東証グロース市場 |
|
業種 |
医薬品 |
|
代表取締役社長 |
森 敬太 |
|
所在地 |
東京都中央区明石町8-1 聖路加タワー13F |
|
決算月 |
1月末日 |
|
HP |
株式情報
|
株価 |
発行済株式数(期末) |
時価総額 |
ROE(実) |
売買単位 |
|
|
1,667円 |
70,927,202株 |
118,235百万円 |
-139.2% |
100株 |
|
|
DPS(予) |
配当利回り(予) |
EPS(予) |
PER(予) |
BPS(実) |
PBR(実) |
|
0.00円 |
– |
-49.41円 |
– |
21.93円 |
76.0倍 |
*株価は4/1終値。各数値は25年1月期決算短信より。
業績推移
|
決算期 |
売上高 |
営業利益 |
経常利益 |
当期純利益 |
EPS |
DPS |
|
2022年1月 |
– |
-6,620 |
-4,579 |
-4,677 |
-90.33 |
0.00 |
|
2023年1月 |
– |
-7,899 |
-4,698 |
-5,559 |
-95.99 |
0.00 |
|
2024年1月 |
– |
-4,539 |
-2,824 |
-2,644 |
-40.48 |
0.00 |
|
2025年1月 |
– |
-3,516 |
-3,022 |
-2,882 |
-41.86 |
0.00 |
|
2026年1月(予) |
– |
-3,509 |
-,3551 |
-,3554 |
-49.41 |
0.00 |
*単位:百万円、円。予想は会社側予想。当期純利益は親会社株主に帰属する当期純利益。(以下、同様)
創業当初に掲げていた2つの目標である「慢性期脳梗塞への対応」と「米国市場での展開」の実現に改めてチャレンジすることを決意したサンバイオグループの「原点回帰の背景と意義」「原点回帰でサンバイオが追い求める世界観(企業価値イメージ)」についてレポートする。
目次
1.原点回帰の背景と意義
2.企業価値推計及び推計のための各種前提条件
3.取材を終えて
サンバイオは当初、アンメット・メディカルニーズの高い慢性期脳梗塞の治療薬開発を目指し、2011年1月に米国において主要開発品「SB623」の慢性期脳梗塞を対象とした臨床試験を開始したが、2019年1月に米国で実施したフェーズ2b試験の解析結果速報において、安全性の問題は認められなかったものの、有効性において統計学的な有意差を示さず、主要評価項目を達成することができなかった。このため、開発リソースの観点から、慢性期外傷性脳損傷プログラムの開発を優先してきた同社だが、「アクーゴ®脳内移植用注」(以下、アクーゴ®)が条件及び期限付き製造販売承認を取得したことから、創業当初に掲げていた2つの目標である「慢性期脳梗塞への対応」と「米国市場での展開」の実現に改めてチャレンジすることを決意した。
再生医療のグローバルリーダーを目指し、「原点回帰」をキーワードに次のステージに向かうサンバイオについて、同社への取材に基づき、「原点回帰の背景と意義」「原点回帰でサンバイオが追い求める世界観(企業価値イメージ)」についてレポートする。
1.原点回帰の背景と意義
(1)背景
開発の中心である日本で得ることができた以下3つのポイントが、「原点回帰」の大きな原動力・背景となっていると思われる。
| ①製品化の実現
アクーゴ®の条件及び期限付き承認を取得し製品化を実現。これにより、「原点回帰」の第一歩である米国展開及び脳梗塞への適応拡大も現実味を帯びている。 |
| ②安定供給体制の確立
アクーゴ®の承認プロセスを経て、製品製造方法及び安定供給体制を確立。加えて、将来の需要増大に備え、JCRファーマ株式会社(東証プライム、4552)とのアライアンスを締結し製造拠点の複線化に目途をつけている。 |
| ③適正な医薬品普及基盤の確立
日本におけるアクーゴ®においては、製品製造から流通、物流、製品プロモーション、疾患啓発など適正な医薬品の普及基盤確立への道筋がついた。これらの経験・学び・ノウハウ、そしてデータ蓄積により、米国展開時の普及体制のスムーズな確立が見込める。 |
(2)意義
「原点回帰」によって生み出される社会的・経済的な意義や価値は以下の通りである。
①より大きな患者規模
外傷性脳損傷は米国では毎年約21万人が発症し、累積の患者数は551万人と推計されている。また、脳梗塞は毎年の発症人数は米国79万人、日本29万人。累積患者数はそれぞれ685万人、119万人と推計されている。
なお、外傷性脳損傷は年齢による発症の特性は無いが、日米とも高齢化が進行する中、脳梗塞は今後、発症患者規模も増大するものと見込まれている。
②アンメット・メディカルニーズへの対応
慢性期脳梗塞及び慢性期外傷性脳損傷患者の運動機能改善を図る医薬品は存在せず、その開発は大きな社会的意義を有する。
③大きな医療経済性
脳梗塞及び外傷性脳損傷により運動機能に障害が生じた場合、障害が一生涯に及ぶ傾向があるため、医療費・介護費に加え、就労できないことから生じるコストも含め、多大な経済損失が発生する。このため、脳梗塞及び外傷性脳損傷による運動機能改善を図る医薬品の価値及び社会貢献度は極めて高い。
④企業価値への貢献
サンバイオの現時点での企業価値は、日本国内におけるアクーゴ®の条件及び期限付き承認とその後の製品発売への期待値で構成されていると思われる。
「原点回帰」により、4年後以降には日米における脳梗塞及び米国における外傷性脳損傷の製品発売を目指す過程において企業価値は大きく増大するものと考えられる。
2.企業価値推計及び推計のための各種前提条件
「原点回帰」が成功した際のサンバイオの企業価値を推計するための各種条件・状況等を以下に整理する。
(1)試算のプロセス
DCFによる企業価値算定にあたっての、各種条件および計算プロセスは以下のとおりである。
<各種条件及び計算プロセス>
| Step1 | 実際にSB623が投与される患者数の推計(今後20年間の推移) |
| Step2 | 薬価の想定 |
| Step3 | 売上高、営業利益、当期利益の予想(今後20年間の推移) |
| Step4 | DCFによる企業価値の算定 |
(2)各ステップにおける計算方法の概要
Step1:実際にSB623が投与される患者数の推計(今後20年間の推移)
1-1総患者数の推計
日米の人口推移予想(UN World Population Prospects: The 2024 Revision)より人口全体及び65歳以上人口の前年増減率を計算。
慢性期脳梗塞は高齢者が多いため65歳以上人口の増減率を用いて、2024年の実績をベースに慢性期脳梗塞患者数の推移を推計。
慢性期外傷性脳損傷に関しては、年齢は考慮せず人口全体の増減率を使用。
1-2 「SB623」投与患者への絞り込み
「SB623」の投与対象患者は、症状、競合状況、浸透率(実際に患者が治療のために来院する比率)により、全ての慢性期患者から絞り込を行い算出。
①症状による絞り込み
あるスケールを用いた運動機能の重症度で「中程度」と判定される患者が主なターゲットとなることを想定。
また慢性期外傷性脳損傷の後遺症には様々な症状が現れるが、「SB623」は言語や記憶、情緒面で日常生活に支障をきたす高次脳機能障害ではなく、自分の意志で筋肉を動かしにくくなる等の「運動麻痺」を対象と想定。サンバイオが社内利用している調査データ(modified Rankin Scale(mRS)やGlasgow Outcome Scale-Extended(GOS-E)等)から、米国慢性期脳梗塞全患者における「中程度患者」及び「運動機能障害」の比率は、それぞれ45%、52%と推計。日本ではそれぞれ57%、66%。
米国の慢性期外傷性脳損傷については、それぞれ69%、33%。
②競合品との関係
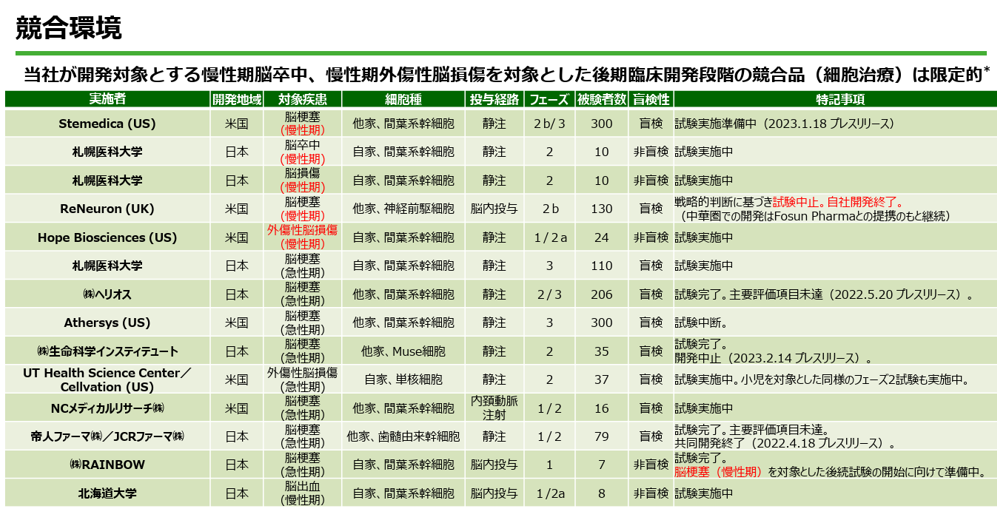
脳梗塞、外傷性脳損傷を対象とした開発中医薬品は下記の表のように、国内外に多く存在するが、サンバイオの「SB623」の特長である以下の2点を考慮すると、競合状況は極めて限定的である。
「慢性期を対象にしていること」
脳梗塞及び外傷性脳損傷には急性期、慢性期があり、再生医療に取り組んでいる他社が主に急性期を対象としているのに対し、同社ではSB623の対象領域を、既存の治療方法では予防・改善効果が限定的でアンメット・メディカルニーズが高い慢性期と設定している。
「他家(たか)移植であること」
再生医療に使用される細胞としては、「自家(じか)移植」と「他家(たか)移植」の2種類がある。
「自家移植」は患者本人から細胞を採取して加工・培養し、元の患者に移植し、治療するため、医薬品の量産化が困難でスケールが望めない。他方、「他家移植」の場合は、健康なドナーから採取した細胞を加工・培養して量産化する。一人のドナーから多くの治療薬を製造することが可能であるため、スケーラブルな展開が期待されている。
(サンバイオ資料より)
この2点を勘案すると、上記の表からは競合は米国の慢性期脳梗塞における米国Stemedica社のみとなる(英国ReNeuron社は自社開発を終了し、中華圏のみで開発継続)。日本の慢性期脳梗塞における競合は存在しない。慢性期外傷性脳損傷に関しては日米とも競合は存在していない。
こうした状況から、慢性期脳梗塞における市場シェアは米国50%、日本100%、慢性期外傷性脳損傷は100%とした。
③浸透率による絞り込み
ただし、薬価、保険制度などの関係から、「SB623」の対象患者がどの程度治療のために来院するかは不透明である。
患者を新たに発症した「発生ベース」と、既に発症している「存在ベース」にカテゴライズし、それぞれの浸透率(実際に投与を受ける患者の構成比)をそれぞれ最大で50%、15%とした(慢性期脳梗塞、慢性期外傷性脳損傷とも同数値)。
以上の想定から毎年実施される治療数を算出する。
*米国:慢性期脳梗塞
米国慢性期脳梗塞総患者数×中程度患者比率(45%)×運動機能障害患者比率(52%)×市場シェア(50%)×浸透率(発生ベース50%、存在ベース15%)
*米国:慢性期外傷性脳損傷
米国慢性期外傷性脳損傷総患者数×中程度患者比率(69%)×運動機能障害患者比率(33%)×投与部位適応率(28%)×市場シェア(100%)×浸透率(発生ベース50%、存在ベース15%)
*日本:慢性期脳梗塞
日本慢性期脳梗塞総患者数×中程度患者比率(57%)×運動機能障害患者比率(66%)×市場シェア(100%)×浸透率(発生ベース50%、存在ベース15%)
Step2:薬価の想定
収支予想を行うための最も重要な要素の一つが薬価である。
サンバイオへの取材で得られた慢性期脳梗塞及び慢性期外傷性脳損傷における医療経済性の観点を考慮し、以下の薬価を想定。
*日本脳梗塞:50,000千円
*米国脳梗塞及び外傷性脳損傷:US500千ドル
米国では遺伝子治療薬において、単回投与でUS2~4百万ドルという超高額製品も販売されていることも確認。
Step3:売上高、営業利益、当期利益の予想
*売上高
売上高は「投与患者数×薬価」となる(「SB623」は単回投与と定められている)。
米国の薬価は1USD=150円で換算。
*コスト
慢性期脳梗塞及び慢性期外傷性脳損傷プログラムを成功させ、日米で販売を開始することで売上・利益とも現在とは比較にならないレベルにスケールした際の同社のコスト構造を推定するにあたっては、2024年度版製薬企業の世界売上高ランキングに基づき、上位10社のコスト構造の平均値を算出した。
それによると、売上原価率は29.7%、販管費率は30.7%、研究開発費率は22.9%となった。
*法人税
40%の前提。
Step4:DCFによる企業価値の算定
4-1成功確率の推計
Step3により今後の売上高、営業利益、当期利益を推計することができるが、DCFによる企業価値算定にあたっては、治験の成功確率による割引が必要になる。
医薬産業政策研究所が2022年に作成した資料によると、細胞薬(Cell therapy)の臨床試験におけるフェーズ別の成功確率は以下のようになっている。
|
総ベンチマーク数 |
成功 |
失敗 |
成功確率 |
|
| PhaseⅠ→PhaseⅡ |
434 |
288 |
146 |
66.4% |
| PhaseⅡ→PhaseⅢ |
342 |
100 |
242 |
29.2% |
| PhaseⅢ→承認申請 |
37 |
20 |
17 |
54.1% |
| 承認申請→承認 |
19 |
19 |
0 |
100.0% |
サンバイオでは米国における慢性期外傷性脳損傷はPhaseⅢからスタートすべく準備中であり、米国および日本の慢性期脳梗塞はPhaseⅡからスタートする予定である。
その場合、以下のように成功確率を推計。
|
対象疾患 |
成功確率 |
| 米国:慢性期脳梗塞 |
15.7% |
| 米国:慢性期外傷性脳損傷 |
54.0% |
| 日本:慢性期脳梗塞 |
15.7% |
4-2 成功確率調整後当期利益の試算
各対象疾患の成功確率調整後当期利益
=当期利益×売上高合計に占める各対象疾患の構成比×各対象疾患の成功確率
「米国:慢性期脳梗塞」「米国:慢性期外傷性脳損傷」「日本:慢性期脳梗塞」の成功確率調整後当期利益合計が、全社の成功確率調整後当期利益となる。
4-3 DCFによる企業価値算定
以上によって求めた全社合計の成功確率調整後当期利益を流列としてDCFモデルにより企業価値を算定する。
WACC(資本コスト)は8.8%とした。
その結果、2026年1月期を初年度とする10年間によって計算した時価総額は5兆6,340億円と算定された。
この数値の取り扱いについては以下を留意する必要がある。
企業価値算定にあたっては、サンバイオが社内利用している各データを受領し、上記のプロセス、計算式に従い計算を行った。前述の通り、多くの前提条件を基にしていること、また、前提条件に加味されていない要素があり得ることも踏まえなければならないことから、この時価総額が当然に想定されると説明するものではない。
あくまでも、サンバイオが「原点回帰」により目指す将来の姿のポテンシャルをイメージしたものである。
リンク:DCFによる企業価値算定の主要条件(抜粋)
https://www.bridge-salon.jp/toushi/wp-content/uploads/2025/03/DCF.pdf
3.取材を終えて
2024年7月、日本において厚生労働省より「アクーゴ®」が、「外傷性脳損傷に伴う慢性期の運動麻痺の改善」を効能・効果として、日本における条件及び期限付き製造販売承認を取得。このころより、同社内は「原点回帰」に向けた機運が大きく高まり、活気に溢れているということだ。
同社が「原点回帰」する先には、上記でイメージしたような大きな企業価値を創造する世界があり、真剣にその世界の実現を目指している。「原点回帰」に臨む慢性期脳梗塞及び慢性期外傷性脳損傷、両プログラムの進捗を今後も注目していきたい。

