(2183)株式会社リニカル 欧州事業増収 利益は米欧ともに改善
 秦野 和浩 社長 |
株式会社リニカル(2183) |
 |
会社情報
|
市場 |
東証プライム市場 |
|
業種 |
サービス業 |
|
代表取締役社長 |
秦野 和浩 |
|
所在地 |
大阪市淀川区宮原1-6-1 新大阪ブリックビル |
|
決算月 |
3月 |
|
HP |
株式情報
|
株価 |
発行済株式数(自己株式を控除) |
時価総額 |
ROE(実) |
売買単位 |
|
|
708円 |
22,586,436株 |
15,991百万円 |
12.9% |
100株 |
|
|
DPS(予) |
配当利回り(予) |
EPS(予) |
PER(予) |
BPS(実) |
PBR(実) |
|
14.00円 |
2.0% |
38.56円 |
18.4倍 |
289.69円 |
2.4倍 |
*株価は12/7終値。発行済株式数は直近四半期末の発行済株式数から自己株式を控除。
*ROEとBPSは22/3月期。EPSとDPSは23/3月期予想。
連結業績推移
|
決算期 |
売上高 |
営業利益 |
経常利益 |
親会社株主帰属利益 |
EPS |
DPS |
|
2019年3月(実) |
11,313 |
1,212 |
1,253 |
568 |
25.09 |
12.00 |
|
2020年3月(実) |
10,935 |
1,005 |
918 |
482 |
21.38 |
14.00 |
|
2021年3月(実) |
10,279 |
453 |
588 |
539 |
23.91 |
14.00 |
|
2022年3月(実) |
11,555 |
1,085 |
1,183 |
790 |
35.00 |
14.00 |
|
2023年3月(予) |
12,440 |
1,224 |
1,204 |
871 |
38.56 |
14.00 |
*単位:百万円
*予想は会社予想。
リニカルの2023年3月期第2四半期決算概要と2023年3月期業績予想について、ブリッジレポートにてご報告致します。
目次
今回のポイント
1.会社概要
2.経営戦略
3.2023年3月期第2四半期決算
4.2023年3月期業績予想
5.今後の注目点
<参考:コーポレート・ガバナンスについて>
今回のポイント
- 23/3期第2四半期は前年同期比7.2%の増収、同26.4%減益。売上面では、欧州事業が前年同期比で増収となったことに加え、為替が円安に推移し海外子会社の収益を押し上げた。利益面では、第1四半期に営業損失を計上したものの、第2四半期は米欧ともに挽回し、欧州は対前年で増益を達成した。
- 第2四半期が終わり、23/3期の会社計画は、前期比7.7%の増収、同12.7%の営業増益の予想から修正なし。受注案件の進捗管理の徹底による売上計上の迅速化と内定案件の早期契約締結・業務開始、および現在交渉中の新規案件獲得による売上高の積み増しを図る。配当も、前期と同額の1株当たり普通配当14円の予想を据え置き。
- 同社は、下期において受注案件の進捗管理の徹底による売上計上の迅速化と内定案件の早期契約締結・業務開始、及び、現在交渉中の新規案件獲得による売上の積み増しに取り組むとともに、受注案件に応じた人件費、経費の厳密なコントロールを実施することにより、通期の会社計画の達成を目指す。第2四半期(7-9月)の収益力の向上が継続するのか、通期の会社計画の達成に向けてどこまで利益を積み上げることができるのか、続く第3四半期の業績動向が注目される。
1.会社概要
臨床試験(治験)に関わる業務の一部を代行する事で製薬会社の医薬品開発を支援するCRO(Contract Research Organization)事業を中心に、医薬品のマーケティング業務ならびに製造販売後(以下製販後という)臨床研究・調査の受託などを行う育薬事業を手掛ける。
医薬品は発売前に厚生労働省の承認・認可を受けることが義務づけられており、承認前の薬剤(医薬品候補)を患者に投与して効果や安全性を確かめる必要がある。その臨床試験としての治験を支援する事業がCRO(Contract Research Organization)である。また、医薬品は製販後も調査、臨床研究を行う必要があり、その段階を支援する事業が育薬(Contract Medical Affairs)である。
同社は創業以来、がん・中枢神経系(CNS)など、世界中の人々がその撲滅を願い、新薬開発への強いニーズが存在する疾病領域を中心にCRO事業を展開してきた。これらは非常に難易度が高い領域であり、同社の知識・経験豊富なエキスパートが高度な治験を支えている。また、同社は創薬支援・育薬事業にも力を注ぎ、申請業務支援、承認後のマーケティングや臨床研究、製販後調査支援まで、単なるアウトソーシングを越えてお客様の事業を幅広くコンサルティングする「製薬会社の真のClinical Development Partner(医薬品開発パートナー)」を目指している。更に、国際化・大規模化が進む医薬品開発の流れのなかで、グローバルで大規模なプロジェクトにも同社グループのワンストップで十分な対応を行い、製薬会社とともに新しい時代を開拓していく戦略的ビジネスパートナーとして、顧客の市場競争力の拡充をトータルに支援している。
また、同社は、受託特化型の事業形態により、特定領域への特化、特定治験段階への特化(フェーズⅡ、フェーズⅢ)を通じて、高収益体質を構築している。
【沿革】
2005年6月、藤沢薬品工業株式会社(現 アステラス製薬株式会社)で免疫抑制剤等の開発に携わってきたメンバー9名によって設立された。大阪発理想の医薬品開発受託(CRO)事業を目的として、設立当初から、CNS領域やがん領域の育成に取り組み、会社設立後まもなく大塚製薬からCNS領域の案件を受注。その後、人材を補強し事業部として受注活動を強化した。また、がん領域も外資系製薬会社等でがん領域の医薬品開発を手掛けた人材等に恵まれ、足元、受注が拡大している。
SMO(治験施設支援機関)事業進出を念頭に、06年1月に同事業を手掛けるアウローラ(株)を子会社化したが、CRO事業への経営資源集中を図るべく07年5月に全保有株式を売却。08年7月に、国内の製薬会社の米国進出支援を目的に米国カリフォルニア州に全額出資子会社LINICAL USA, INC.を設立。同年10月の東証マザーズ上場を経て、13年3月に東証1部に市場変更となった。13年5月に、台湾と韓国に全額出資子会社LINICAL TAIWAN CO., LTD.とLINICAL KOREA CO., LTD.を設立。14年4月には、LINICAL KOREA CO., LTD.と買収した韓国のCROであるP-pro. Korea Co., Ltd.との統合を完了した。14年10月29日には欧州でCRO事業を展開しているNuvisan CDD Holding GmbHの全株式を取得し子会社化するための株式譲渡契約を、Nuvisan Pharma Holding GmbH との間で締結し、12月1日付けで同社の100%子会社となった。更に、グループとしての一体感の醸成と連携強化を図るため、連結子会社となったNuvisan CDD Germany GmbHの名称をLINICAL Europe GmbHに商号変更した。その他、16年3月にLINICAL U.K. LTD.を、同年10月にLINICAL POLAND Sp.z.o.o.を、17年9月にLINICAL Czech Republic s.r.o設立した。また、2018年4月に米国でAccelovance, Inc.を買収し、Linical Accelovance America, Inc.に社名変更。その他、19年3月にLinical Hungary Kft.を設立、19年5月にLinical China Co., Ltd.を設立した。更に、2019年12月にLINICAL Europe GmbHへLAA社の欧州子会社を統合し欧州地域の強化を図ったことに加え、20年2月に上海支店を開設し国際共同治験の受託体制が更に強化された。また、20年4月にLinical Benelux B.V と Linical Accelovance Europe B.V. を合併し、Linical Netherlands B.Vを発足、23年3月期にはLinical China Co., Ltd. とLinical Accelovance China Ltd.の統合を予定している。
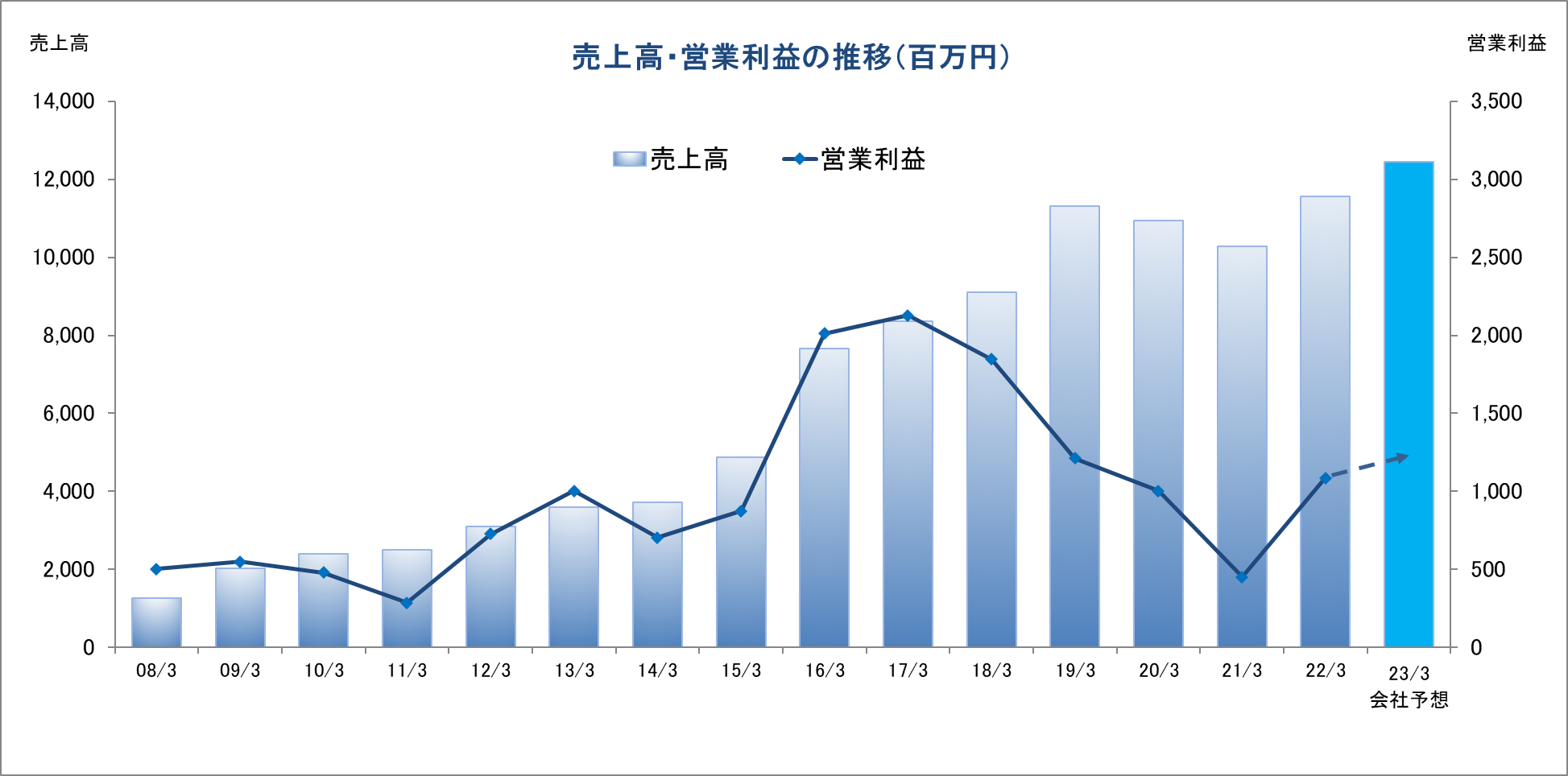
世界各地で新型コロナ感染症拡大の影響が残る中、2022年3月期は過去最高の売上高を記録するとともに、営業利益も新型コロナ感染症拡大前の水準へ回復した。
【業務内容】
同社は、主にCRO事業(臨床開発事業)、製造販売後の臨床試験や臨床研究とマーケティング活動支援を担当する育薬事業、創薬支援事業を展開している。非臨床試験段階から臨床開発、製造販売後の育薬まで一気通貫で対応出来る体制をとることで、効率的な新薬開発による上市までの期間の短縮や製品ライフサイクルの延長を可能とし、製薬会社の真のパートナーとして医薬品の価値最大化に貢献している。更に、同社は、製薬会社のみならずバイオベンチャーに対して、ライセンス等の出口戦略まで多面的に支援している。
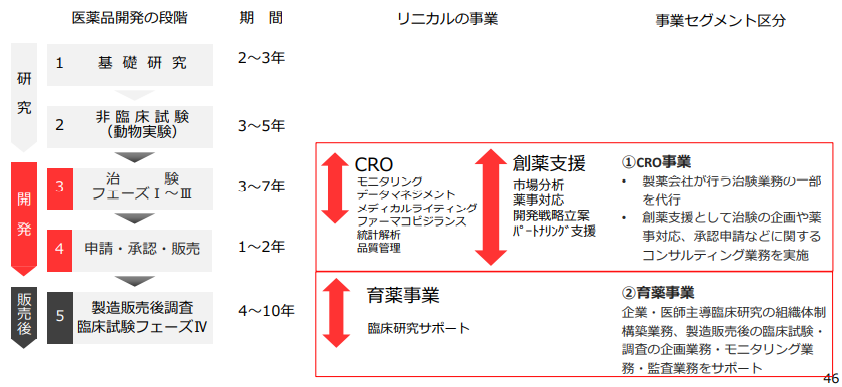
(同社決算説明会資料より)
CRO事業(臨床開発事業)
CRO事業は、製薬会社が行う治験業務の一部を代行する事業で、モニタリング、データマネジメント、メディカルライティング、ファーマコビジランス、統計解析、品質管理などの業務を行っている。同社では、新薬の迅速な市場投入につながる高品質で高効率な治験の支援を目指して、高い技術と豊富な経験をもつスタッフが担当にあたっている。今後も拡大するグローバルスタディに対応していくため、アジア(韓国、台湾、シンガポール、中国など)と欧州、米国に拠点を開設。薬事から企画、実施計画書の作成、モニタリング、データマネージメント、統計解析、ファーマコビジランスまでワンストップで対応。国際共同治験においては、リニカル本社を窓口に位置づけ、各国に医薬品開発事情に精通した人材を配置。日本語ベースで機動的な国際共同治験が可能な開発環境を整えている。10年から20年近くに及ぶ新薬開発プロジェクトの中でも、3年から7年を要するといわれる治験で特に重要とされる患者を対象とする「第Ⅱ相(フェーズⅡ試験)」「第Ⅲ相(フェーズⅢ試験)」のプロセスに特化し、受託特化型の事業形態にて治験の核となる「モニタリング」を「品質管理」「コンサルティング」とともに提供。信頼性の高いデータの収集を行い、迅速、確実な新薬開発の実現を支援している。更に、豊富な医薬品開発情報を有する大手製薬会社に特化すると共に、担当領域も市場からの開発要請の強いがん領域や中枢神経系領域をはじめ難易度の高い領域に特化することで、顧客である製薬会社のニーズに応えている。
また、同社は、スケジュール管理、治験標準業務手順書・GCP遵守、データ・症例報告書の信頼性などの分野におけるサービスクオリティの高さに強みを持っている。
*国際共同治験
「国際共同治験」とは、新規の医薬品開発に世界規模で取り組み、早期上市を目指すため、臨床試験を複数の国または地域において同時並行的に行うことをいう。
*GCP(Good Clinical Practice)
「GCP」とは治験を実施する際に守るべきルールで、日本で正しく治験を実施できるように厚生労働省により省令(法律を補う規則)として定められているもの。
育薬事業
育薬事業は、企業・医師主導臨床研究の組織体制、構築業務、製造販売後の臨床試験・調査の企画業務・モニタリング業務・監査業務をサポートする事業であり、同社は臨床研究のサポートを実施している。臨床研究法が施行され臨床研究を取り巻く環境は大きく変化している中、情報をタイムリーにキャッチアップし、製薬会社のメディカルアフェアーズ部にとって最良のパートナーとなれるよう、臨床研究のモニタリング・研究事務局業務を中心にデータマネジメント・統計解析などを含めたフルサービスの支援を行っている。J-GCPだけでなく、倫理指針、臨床研究法に加えてICH-GCP準拠の臨床試験も対応しており、全てのレギュレーションでのサービスを提供している。また、当初よりPrimary領域、中枢神経領域でのサービスを提供。現在はがん領域を強化し、半数以上のモニターががん領域の経験者となっている。開発で培ったノウハウをベースに、最新のレギュレーションに対応し、難易度の高い領域でエビデンス創造に貢献する方針である。
創薬支援事業
既存の臨床開発事業と育薬事業に続く、第3の事業である創薬支援事業 (Innovative Drug Development Business) を展開中。創薬支援事業では、市場分析、薬事対応、開発戦略立案、パートナリング支援などの業務を行っている。国内大手製薬会社でライセンス、事業開発、臨床開発、開発薬事、マーケティングといった業務に携わり、開発品の目利きから、導入・導出交渉、臨床開発などで数々の実績と豊富な経験を有している担当者が中心となり、主に①開発品の市場分析、②薬事相談のサポート、③ライセンスのサポートの3種のコンサルティングサービスを提供している。これらの経験を武器に、現在、国内または国外の製薬会社、バイオテクノロジーカンパニーからの業務を開発早期より支援している。今後、更に同社の国際拠点と連携し、グローバルでトータルにサポートできる体制を進める方針である。
【5つの強み】
(1)グローバル規模でワンストップ
同社は日本発のグローバルCROとして、日本を中心にアジア、欧州、米国の3極でサービスを提供可能であり、医薬品開発のプロフェッショナルとして新薬開発に貢献している。創業当社から積極的に海外進出し、現在、18か国/地域に事業展開し、世界20程度の国/地域でサービス提供が可能である。また、医薬品開発のプランニングから、モニタリング、データマネジメント、統計解析、メディカル・ライティング、薬事、ファーマコビジランスなどあらゆるサービスにおいて経験豊富なプロフェッショナル・メンバーが顧客ニーズに応え、Local試験はもちろん、マルチナショナル・トライアルまでフルサービス、且つ、ワンストップで提供している。
LINICAL Global 拠点 「日本・アジア+米国+欧州」の3極体制
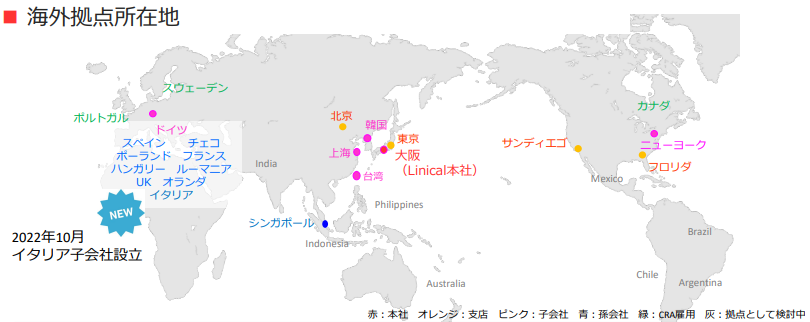
(同社決算説明会資料より)
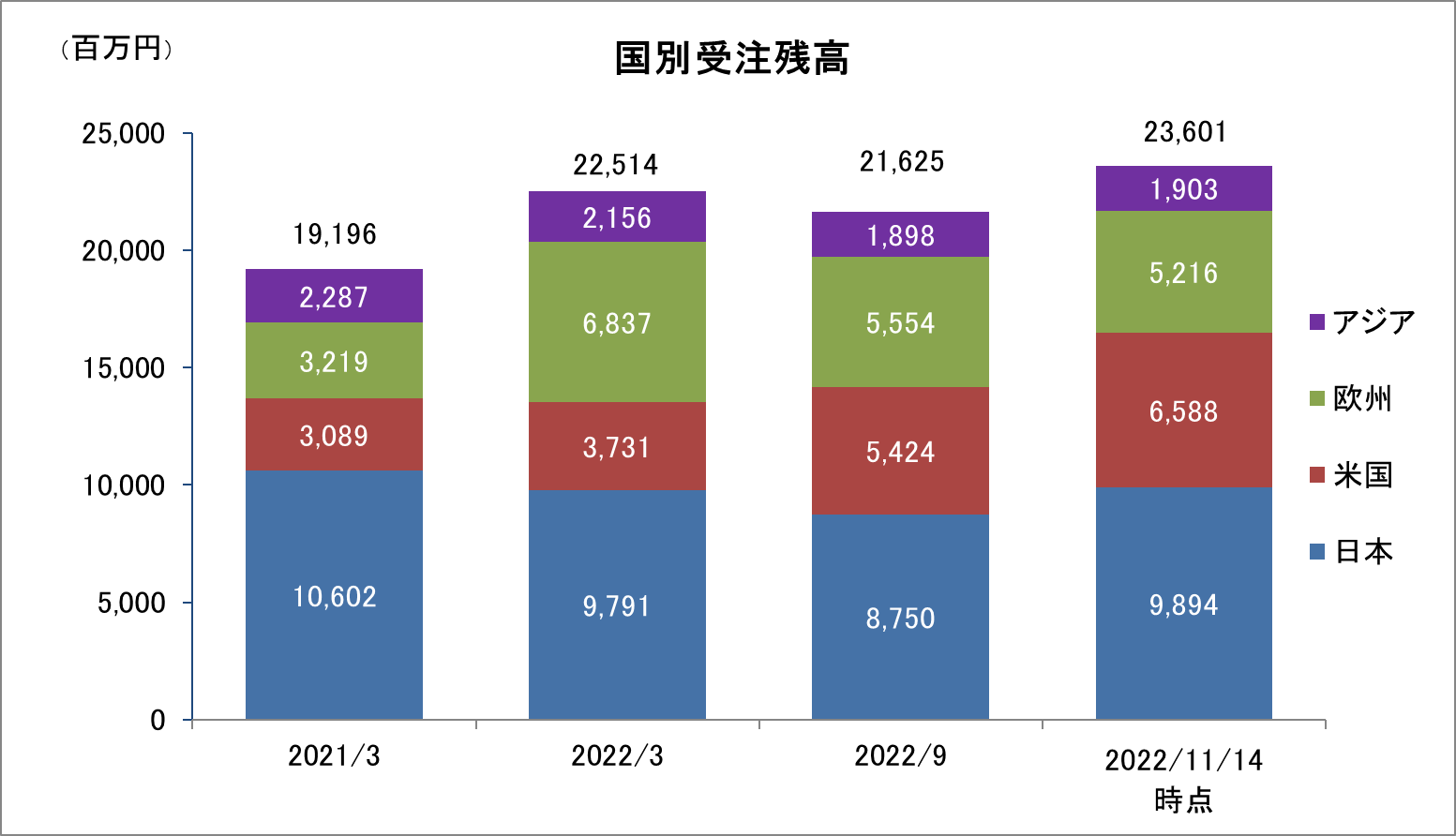
日本・アジア+米国+欧州の3極体制整備の成果により、新規案件の受託が順調に増加している。特に日本と米国における大型の新規案件の獲得などにより、2022年11月14日時点の受注残高は236億円まで積み上がっている。なお、現在受注の内定を受け契約締結交渉中の案件を含めると、実質的な受注残高は250億円を超える水準となっている模様である。
(2)創薬支援から臨床開発、臨床研究まで
同社はCSR(corporate social responsibility)として、医薬品開発業務の一端を担う会社として社会に貢献したいと考えている。更に、同社は顧客の真のパートナーとして薬剤の価値最大化に貢献するべく、創薬段階から臨床開発、製造販売後の育薬まで一気通貫で対応出来る体制をとることにより、効率的な新薬開発とライフサイクルマネジメントの延長を可能とし、上市までの期間の短縮(TTM)と売上の早期最大化(TTP)を図っている。日本においては創薬支援事業で創薬支援を、臨床開発事業(CRO事業)では臨床開発を、臨床研究支援事業では製造販売後の臨床試験や臨床研究をサポートしている。
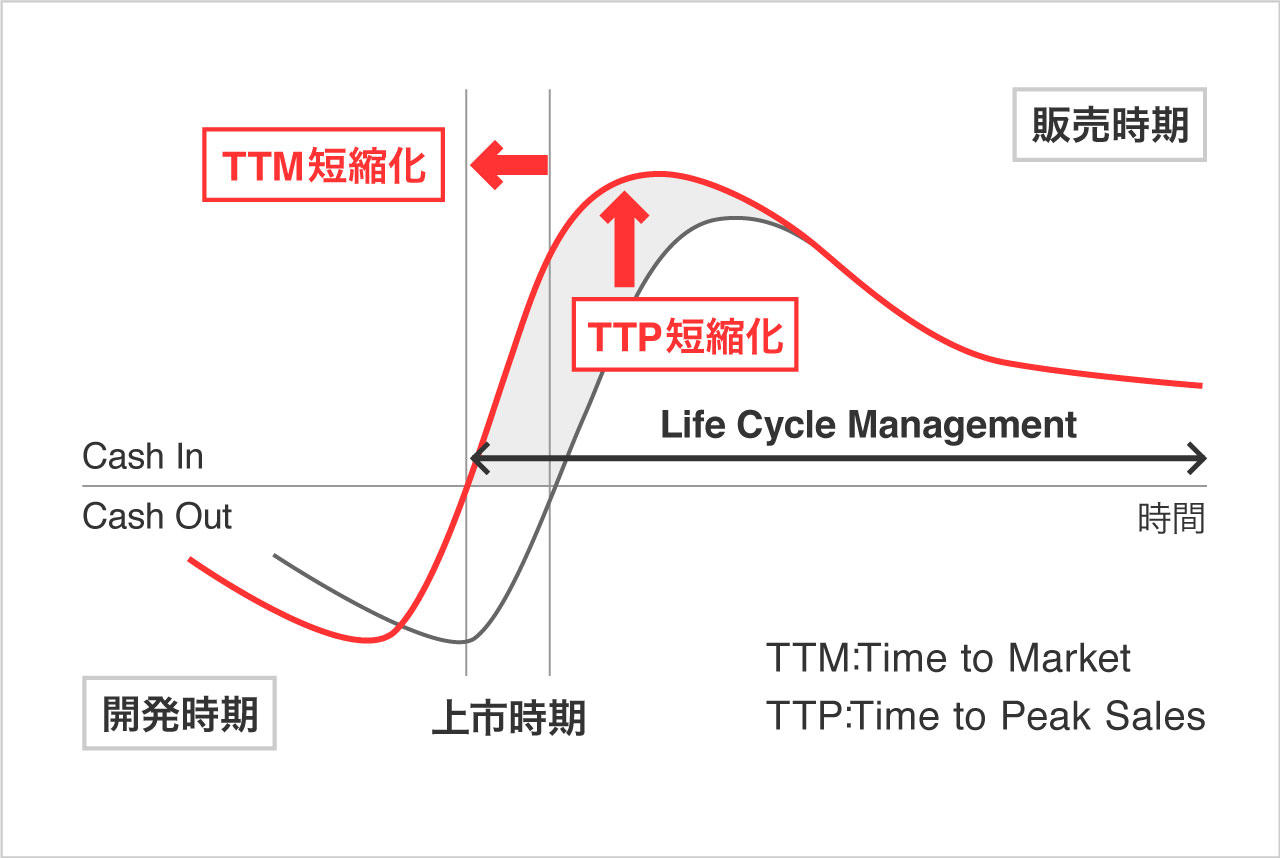
(同社HPより)
(3)がん・中枢・免疫にフォーカス
医薬品開発のトレンドは、がん、中枢神経系、免疫領域に集中してきている。同社創業メンバーは免疫領域において豊富な経験を持ち、創業当初より難易度の高い免疫領域等を中心にサービスを提供してきた。その後、日本においては2006年に中枢神経領域、2010年にがん領域へと専門性を拡げていき、現在では難易度の高い、がん、中枢神経系、免疫などアンメット・メディカル・ニーズな領域でのサービスを大きな3本柱として事業を展開している。また、海外子会社においても同じく、がん、中枢神経系、免疫系のサービス実績が多く、同社全体で難易度の高いがん、中枢神経系、免疫系を得意領域としている。更に、今後成長が見込まれる皮膚科領域や眼科領域に加え、難易度の高い再生医療領域も今後のサービスの大きな柱にするべく、準備を進めている。
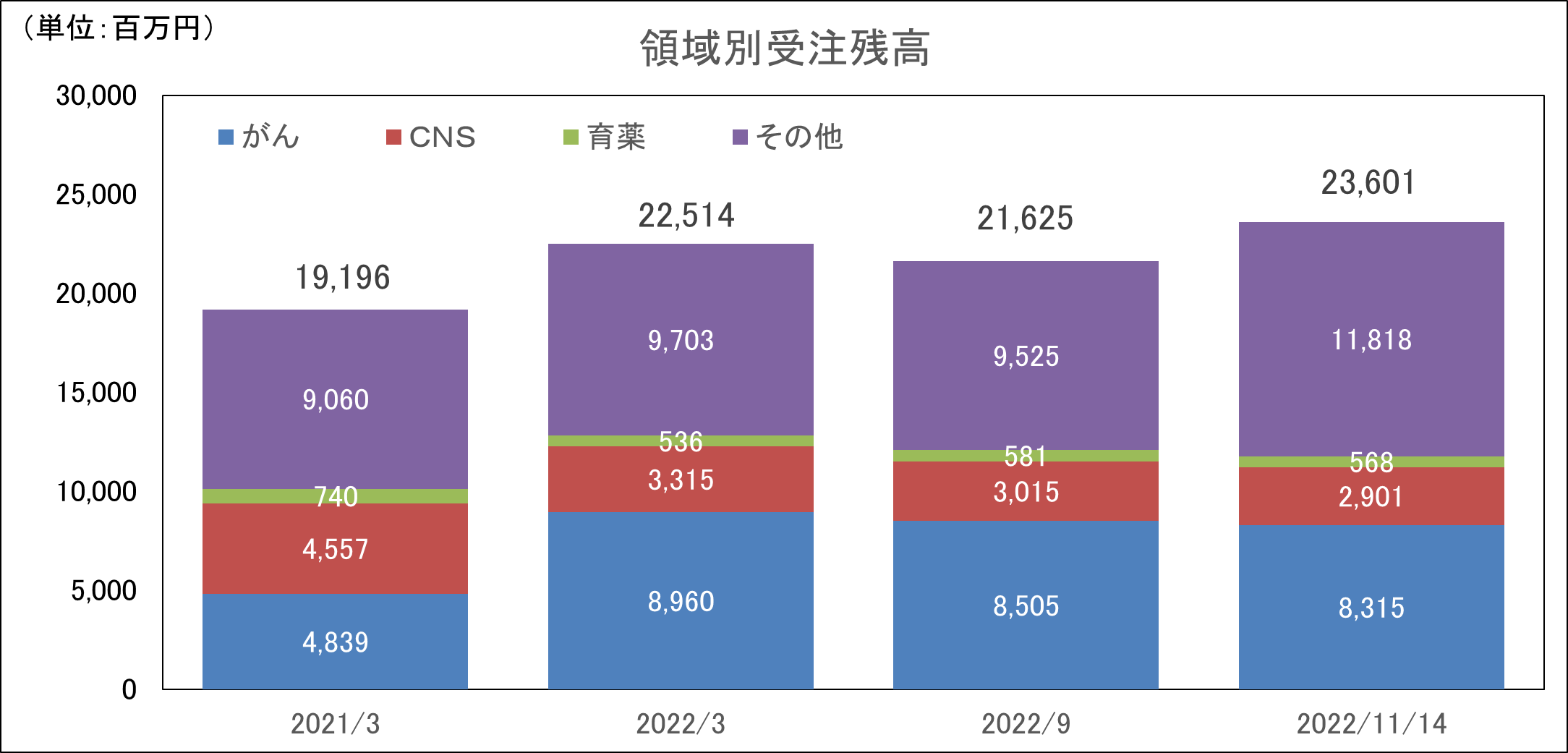
2022年11月14日時点の受注残高は過去最高水準にあるが、主力のがん、中枢神経系が高水準を維持する中、その他領域の拡大が著しい。
(4)グローバル・コラボレーション
日本発グローバルCROとして、顧客へ世界規模のサービスを提供。高品質(Japan Quality)なサービスを提供する為に、日本に国際事業開発本部を設置し、日本語、英語、母国語を含めたその他言語(韓国語、中国語、ドイツ語など)が堪能なマルチリンガル・メンバーを大阪本社および東京支社に多数配置し、海外メンバーと適切なコミュニケーションをとっている。日本の顧客とは日本語でのコミュニケーションも可能。海外メンバーもJapan Qualityについて理解を深めており、All LinicalとしてJapan Qualityを提供している。
日本発の日台韓Asia試験の実施体制の一例として、日本にProject Managerを配置し、日台韓のLeaderを日本に配置するケース、各国拠点にLeaderを配置するケースなど、顧客ニーズに沿った提案があげられる。また、日本発の日米試験やEUとアジア、EUと米国との共同試験も多数実績があり、顧客の開発戦略に合わせた世界規模での提案が可能。
(5)高品質なサービス
同社は顧客へ高品質なサービスを提供すべく、社員に対して量・質ともに充実した教育を実施。その成果として、一般社団法人日本臨床試験学会による GCP サポート認定試験にて第 1 回目から高い合格率を維持しており、当学会より高い合格率と質の高い臨床試験の推進に貢献した証として感謝状を授与された。また、GCP 適合性調査の経験が豊富にあり、FDA inspectionの経験もある。いずれも適合・問題無しとの評価を受けており、同社の品質については社外からも高い評価を得ている。なお、海外子会社においても、FDA や KFDA 、ANVISA などからの inspection の経験があり、日本同様に高い評価を得ている。同社は、高品質とスピードを両立して最高のサービスを顧客に提供することが最大の使命と強く認識している。
2.経営戦略
IQVIA 「The Global Use of Medicines 2022 OUTLOOK TO 2026 」によると、 世界の医薬品市場は2021年の1兆4,230億米ドルから2026年には1兆7,500~1兆7,800億米ドルまで年平均3-6%で成長見込みとなっている。その中で、米国の市場規模が全体の40.2%を占め、欧州(イギリス・ドイツ・フランス・イタリア・スペイン)が15.4%、中国が12.4%、日本が5.2%を占める予想となっている。世界の医薬品市場の拡大とともに、今後CRO市場も拡大が予想される。こうした中、日本は先進国で唯一マイナス成長の予測となっており、世界最大市場である米国を始めグローバルでの事業拡大が必須となっている。
【地域別売上高と従業員数(2022年3月末)】

【第2目標】
①日本500人、アジア400人、欧州400人、米国400人、1500人を超える体制の構築
②各極で成長投資(M&Aを含む)を行いつつ黒字維持、利益率の向上
③世界60ヵ国程度への進出。時差を考慮しつつ、日米欧それぞれの地域でカバーエリアの拡大を検討。南半球に拠点を持つことで、季節性疾患の臨床試験を一年中実施することが可能となる。
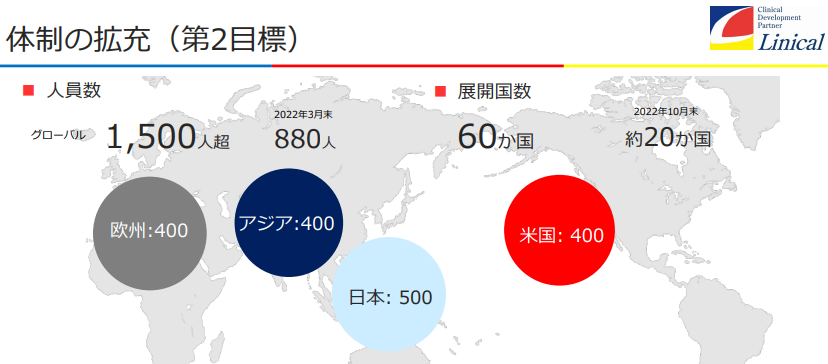
(同社決算説明会資料より)
(1)日本の戦略
国内の市場環境においては、治験数は横ばいで国際共同治験の割合が増加している。
こうした中、以下の重点項目へ注力する。
◆グローバルCRO事業基盤拡大による、国際共同治験における日本試験の獲得
◆創薬事業:第3の柱に
◆CRO事業:対象顧客、疾患領域、サービス内容の拡充
◆育薬事業:環境変化をとらえ再び成長軌道へ
【CRO事業】
|
初期 |
現在 |
|
|
顧客 |
国内大手製薬会社 |
国内大手製薬会社 海外大手製薬会社 国内外のバイオベンチャー |
|
疾患領域 |
がん領域 CNS領域 免疫領域 |
がん領域 CNS領域 免疫領域 眼科領域 皮膚科領域 再生医療 |
|
サービス |
モニタリング |
モニタリングプロジェクトマネジメント 品質管理/監査 データマネージメント メディカルライティング ファーマコビジランスなど |
(同社決算説明会資料より)
従来は、国内大手製薬会社が中心であったが、フルサービスの提供を通じて海外大手製薬会社や国内外のバイオベンチャーにおけるシェアアップを図る。また、がん領域、CNS領域、免疫領域に加え、再生医療、皮膚科、眼科領域を強化する。また、顧客・疾患領域・サービスの各面からビジネスモデルを進化させ、中長期的な成長と収益力向上を目指す。更に、再生医療、治療アプリなど今後拡大が見込まれる最新の治療法にも先駆けて取り組む予定である。
【育薬事業】
同社は、2011年より臨床研究支援のパイオニアとして、大規模臨床研究の支援を開始した。250施設を超える大規模介入臨床研究(後の特定臨床研究)や日台韓のグローバル臨床研究など様々な形態の研究の実績を蓄積した。更に、グローバル組織との連携により、グローバルなニーズに合わせた体制での実施も可能である。
医薬品の製造販売後に行われる試験は、医薬品が実際に患者に投与される中での安全性や効果等を調査・研究するために実施される。コントロールされた環境下で行われる治験とは違い、日常診療の環境で収集された患者の日常の様々なデータ(電子カルテ、レセプト(診療報酬情報)、健康診断、ウェアラブルデバイスなど)を用いたリアルワールドデータ(Real World Data、RWD)を使用する。
このリアルワールドデータ活用のメリットとしては、①医薬品開発プロセスの効率化、②医療施設の負担軽減、③希少疾病、難病などの無作為化比較試験(プラセボ)の実施が困難な領域の開発が促進があげられる。今後リアルワールドデータの医薬品開発への利活用が活発化するものと予想される。一方で、医療データへのアクセス制限、データの標準化、データの連結などに加え、承認申請に使用するための「データの品質」の確保がリアルワールドデータ活用の課題となっている。
同社では、製販後試験の在り方の変化に伴い、リアルワールドデータ活用上の課題であるデータの品質を確保するためCROへの役割期待が増し、ビジネスチャンスが今後拡大すると想定している。
<RWD活用に関する日米欧の規制当局の動き>
|
欧州(EMA) |
米国(FDA) |
日本(PMDA) |
| ◆市場に出回っている製品について、初回製造販売承認の40%にRWE(リアルワールドエビデンス)が含まれる。
◆2025年までに、欧州における医薬品の開発・承認・監督に関する規制当局の意思決定に、RWEを利用しその価値を確立することを目指した活動が進捗。 |
◆2016年にThe 21st Century Cures Actが可決。
◆薬の適応追加に関する規制当局の意思決定をサポートするため、RWD・RWEを利用することに重点を置く。 ◆活用のための各種ガイダンスも整備済み。 |
◆2021年よりRWD WGを創設。
RWD活用に関する基本的考え方および信頼性の担保に関する考え方を検討中。 ◆レジストリデータ等の医薬品の承認申請、再審査等申請に利用する体制構築を進めている(レジストリ・データベースに関する対面助言など)。 ◆最近では、TS-1の特定臨床研究データで適応追加申請が承認。 |
グローバルでリアルワールドデータの活用が進展中である。
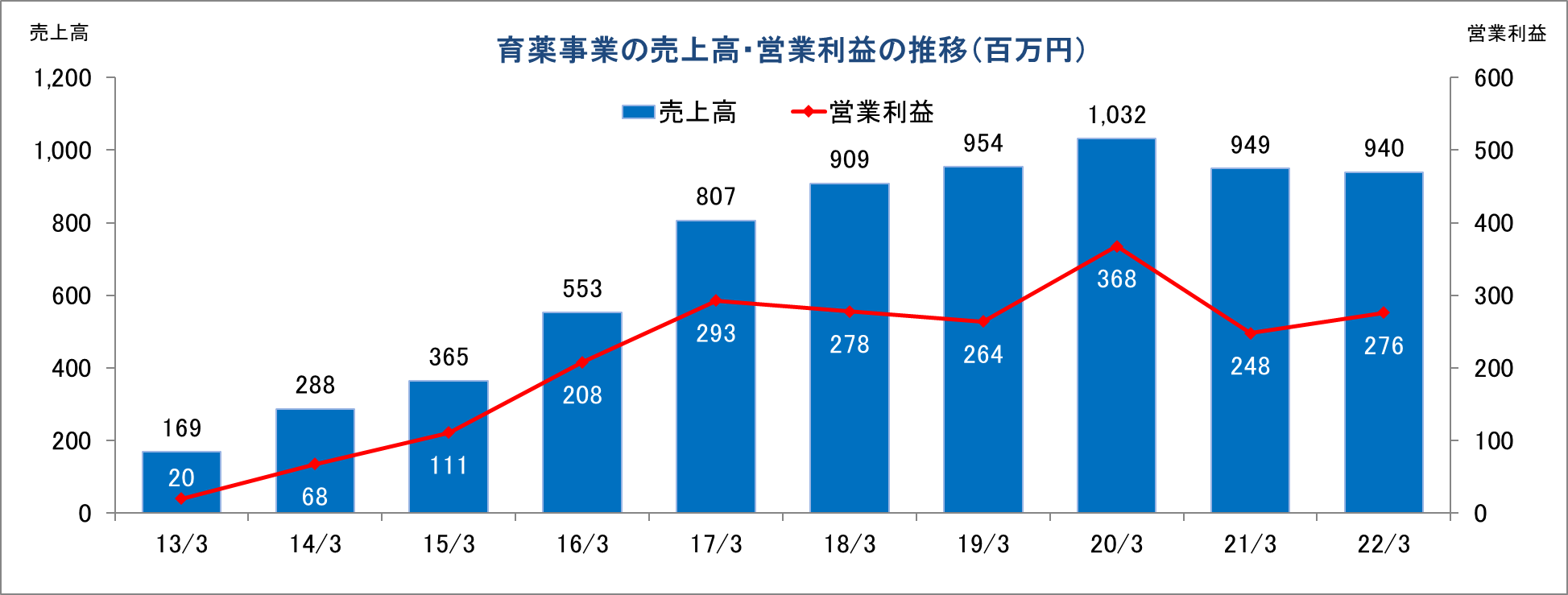
(注)16/3期第1四半期連結会計期間より従来のセグメントの名称を「CSO事業」から「育薬事業」へ変更した。
また、同社は、ウェアラブルデバイスなどのe-Sourceを用いたDCT (分散型臨床試験/ Decentralized Clinical Trial)の取り組みも推進しており、DCTパートナーも国内外で拡充中である。
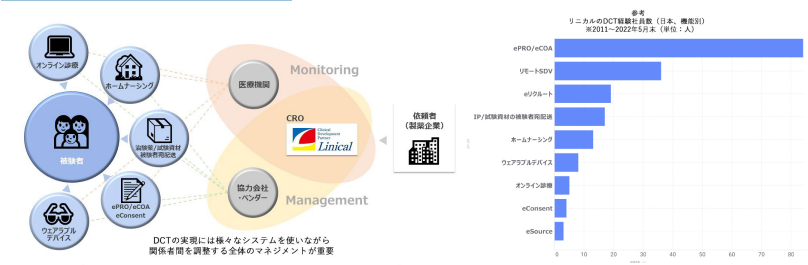
(同社決算説明会資料より)
【創薬支援事業】
同社は、既存の臨床開発事業と育薬事業に続く、第3の事業である創薬支援事業 (Innovative Drug Development Business) を展開している。国内大手製薬会社でライセンス、事業開発、臨床開発、開発薬事、マーケティングといった業務に携わり、開発品の目利きから、導入・導出交渉、臨床開発などで数々の実績と豊富な経験をしている人材が中心となり、主に①開発品の市場分析、②薬事相談のサポート、③ライセンスのサポートの3種のコンサルティングサービスを提供している。
それらの経験をもとに、現在、日本、韓国、台湾の製薬会社、バイオテクノロジーカンパニーからの業務を開発早期より支援しており、今後、更に同社の国際拠点と連携し、グローバルでトータルにサポートできる体制を推進する方針である。
<3種のコンサルティング>
日本の医薬品市場に参入し、自社製品を流通・販売したいが、日本の市場や薬事の知識が十分でない、十分な開発・販売機能を備えていない、戦略的パートナー/ライセンシーを必要としている国内外のバイオテック・ベンチャー・カンパニー/中堅ファルマ対し、同社では以下のサービスを提供している。
|
市場分析/調査 |
・対象疾患の疫学調査
・市場価値と動向予測 ・現行治療アルゴリズムとガイドライン調査 ・承認薬と開発パイプライン調査 ・目標とする製品性能(TPP)立案 ・公定薬価とピークセールス予測、収益性評価 |
|
薬事・ 開発戦略 PMDA相談 (MW) |
・開発/薬事戦略の立案と提案
・PMDA相談のための資料作成、申し込み、会議出席、照会事項対応 ・治験薬概要書、プロトコル、同意文書等の作成 ・治験届と照会事項対応 ・治験国内管理人業務 ・オーファン薬の登録申請 ・Common Technical Document(CTD)作成 |
|
戦略的提携/ ライセンス |
・提携候補会社/ライセンシーの調査と分析
・提携候補会社/ライセンシーとの面談、製品/技術の説明 ・パートナリング目的のカンファレンスへの参加 ・Due Diligenceのサポート ・契約交渉のサポート |
<ドラック・ロスへの取り組み>
ドラッグ・ラグとは、海外ですでに承認されている薬が日本国内での薬事承認を得るまでに長い年月を要する問題である。 これには二つの側面があり、日本で発売している薬が承認までに要した期間が他の国よりも長い「ラグ(遅延)」の問題と、他国で発売されているのに日本では発売されていない「国内未承認薬」の問題がある。特に後者において、国内未承認薬の品目数、割合は増加傾向にあり、日本に海外の新薬が入ってこない「ドラッグ・ロス」の懸念が生じている。
こうした背景には、様々な要因が考えられるが、その一つに、海外新興バイオ医薬品企業が台頭しており、新規有効成分の申請・販売に占める新興バイオ医薬品企業の比率が拡大していることがある。これら新興バイオ企業は日本にオフィスを持たない場合も多い。このように、内外のバイオテック・ベンチャー、中堅製薬会社の中には、日本の医薬品市場に参入し、自社製品を流通・販売したいが、日本の市場や薬事の知識が十分でない、十分な開発・販売機能を備えていない、戦略的パートナーやライセンシーを必要としている企業が数多くある。こうした問題を解決すべく、大手製薬会社やアカデミアで、医薬品開発に関わる広範囲な業務を長年経験したプロフェッショナル集団である同社の創薬事業部を筆頭に、日本発グローバルCROとして、日本のドラッグ・ロスを防ぐために継続的に取り組む方針である。
(2)アジアの戦略
中期の業績目標は、売上高15億円、営業利益率15%。また、前期末の131名の人員を早期に200名まで拡大し、長期では自前の拡大にて400名体制を検討する。具体的な戦略としては、中国市場の開拓を進める。
(3)欧州の戦略
中期の業績目標は、売上高30百万ユーロ、営業利益率15%。また、前期末の209名の人員を早期に300名まで拡大し、長期では自前とM&Aも活用した拡大にて400名体制を検討する。現在進めている具体的な施策としては、イタリア拠点の設立(2022年10月完了)や英国の拡充を予定している。
(4)米国の戦略
中期の業績目標は、売上高30百万米ドル、営業利益率15%を達成する。また、前期末の105名の人員を早期に150名まで拡大し、長期ではM&Aも活用した拡大にて400名体制を検討する。具体的な戦略としては、台頭している海外新興バイオ医薬品企業(Emerging Biopharma=EBP)に照準を定める。
3.2023年3月期第2四半期決算
(1)連結業績
|
22/3期 第2四半期 |
構成比 |
23/3期 第2四半期 |
構成比 |
前年同期比 |
||
|
売上高 |
5,522 |
100.0% |
5,920 |
100.0% |
+7.2% |
|
|
売上総利益 |
1,676 |
30.4% |
1,840 |
31.1% |
+9.8% |
|
|
販管費 |
1,169 |
21.2% |
1,467 |
24.8% |
+25.5% |
|
|
営業利益 |
507 |
9.2% |
373 |
6.3% |
-26.4% |
|
|
経常利益 |
496 |
9.0% |
614 |
10.4% |
+23.9% |
|
|
親会社株主に帰属する四半期純利益 |
252 |
4.6% |
468 |
7.9% |
+85.6% |
|
*単位:百万円
*数値には(株)インベストメントブリッジが参考値として算出した数値が含まれており、実際の数値と誤差が生じている場合があります。(以下同じ)
前年同期比7.2%の増収、同26.4%の営業減益
売上高は前年同期比7.2%増の59億20百万円、営業利益は同26.4%減の3億73百万円。
売上面では、欧州事業が前年同期比で増収となったことに加え、為替が円安に推移し海外子会社の収益を押し上げた。
利益面では、ロシア・ウクライナ戦争等の影響により米欧地域での大型国際共同試験の開始が遅れ、一時的に要員稼働率が低下したことなどにより第1四半期では営業損失を計上したものの、第2四半期では欧州と米国事業がともに改善した。遅れていた大型試験は、ロシアで予定されていた治験施設を欧州各国へ振り分ける等の調整が長引いたものの、7月後半には開始され、以降はおおむね順調に進捗している。売上総利益率は31.1%と前年同期比0.7ポイント上昇した。一方、販管費が前年同期比25.5%の大幅な増加となった。その他、営業外収益で外貨預金等に為替差益が2億65百万円(前年同期は為替差損1百万円)発生した等により、経常利益は前年同期比23.9%増の6億14百万円に拡大した。また、特別利益で受取保険金を50百万円計上したことや前年同期に特別損失で計上した仲裁関連費用1億8百万円が今上期は発生しなかったことなどにより、親会社株主に帰属する四半期期純利益は、前年同期比85.6%増の4億68百万円となった。
セグメント別売上高・利益
|
22/3期 第2四半期 |
構成比 売上高営業利益率 |
23/3期 第2四半期 |
構成比 売上高営業利益率 |
前年同期比 |
||
|
CRO事業 |
5,138 |
93.0% |
5,468 |
92.4% |
+6.4% |
|
|
育薬事業 |
384 |
7.0% |
451 |
7.6% |
+17.7% |
|
|
連結売上高 |
5,522 |
100.0% |
5,920 |
100.0% |
+7.2% |
|
|
CRO事業 |
1,190 |
23.2% |
1,014 |
18.6% |
-14.8% |
|
|
育薬事業 |
126 |
32.8% |
164 |
36.3% |
+30.1% |
|
|
調整額 |
-809 |
– |
-805 |
– |
– |
|
|
連結営業利益 |
507 |
100.0% |
373 |
100.0% |
-26.4% |
|
*単位:百万円
CRO事業では、売上高が54億68百万円と前年同期比6.4%増加し、営業利益が10億14百万円と同14.8%減少した。セグメント利益率は、18.6%と前年同期比4.6ポイント低下した。
育薬事業では、売上高が4億51百万円と前年同期比17.7%増加し、営業利益が1億64百万円と同30.1%増加した。セグメント利益率は、36.3%と同3.5ポイント上昇した。
(2)地域別業績動向
地域別業績動向
|
23/3期 上期 |
||||||
|
売上高 |
前年同期比 |
営業利益 |
前年同期比 |
経常利益 |
前年同期比 |
|
| 日本 |
2,912 |
-4.8% |
341 |
+25.8% |
537 |
+83.4% |
| 米国 |
1,407 |
+17.8% |
42 |
-78.4% |
25 |
-86.2% |
| 欧州 |
1,862 |
+27.8% |
120 |
+38.0% |
157 |
+119.8% |
| 韓国 |
408 |
+20.9% |
36 |
-42.5% |
67 |
-15.8% |
| 台湾 |
63 |
+9.0% |
-15 |
– |
-15 |
– |
| 中国 |
201 |
+6.4% |
21 |
-39.8% |
14 |
-46.2% |
| 連結調整 |
-933 |
– |
-172 |
– |
-171 |
– |
| 合計 |
5,920 |
+7.2% |
373 |
-26.4% |
614 |
+23.9% |
*単位:百万円
*のれんの償却費用は連結調整に含めている。
*売上高は内部取引控除前の数値。
【日本】
日本は、依頼者事由による治験開始時期の変更等により減収となった。一方、採用数調整による人件費等の厳密なコントロールにより前年同期比で増益となった。
【米国】
米国は、第1四半期の米欧地域での大型国際共同試験の遅れ等があったものの第2四半期では改善したことに加え、円安の影響もあり増収となった。また、上記試験の遅れ等に伴う一時的な要員稼働率の低下に加え、新規案件の開始及び工数追加に対応するための増員による人件費の増加があり、第2四半期では稼働率が改善したものの、上期累計では前年同期比で減益となった。
【欧州】
欧州は、前期の好調な受注を消化して売上を計上するとともに、上述の試験開始が遅れた米欧地域での大型国際共同治験でも第2四半期に大きな進捗があったことから、前年同期比で増収増益となった。
【アジア】
韓国は、複数の新規案件を獲得・開始したこと等に加え円安の影響もあり前年同期比で増収となった。利益面では第1四半期に新規案件に対応するための増員による先行的な人件費増加により営業損失を計上した影響が大きく、第2四半期では前年同期比で増益となったものの上期累計では減益となった。
中国は、ゼロ・コロナ政策によるロックダウンの影響から一部の受注案件で進捗が遅れたものの、円安の影響により前年同期比で増収、減益となった。台湾は、既存の一部受注案件でコロナの影響から治験の進捗が遅れたこと等から現地通貨ベースでは前年同期比で減収となったものの、費用節減を進めた結果、営業赤字は大きく減少した。
【のれんの残高と残存償却期間(2022/3期末)
|
金 額 |
残存償却期間 |
年間償却額※4 |
|
| 韓国 |
19/3期で償却終了 |
||
| 欧州 ※1、2 |
1,349 |
11-12年 |
120 |
| 米国 ※1,3 |
2,056 |
12年 |
171 |
*単位:百万円
※1 Linical Accelovance America, Inc.(以下、 LAA )買収により発生したのれんについて、その欧州子会社分を欧州に按分。
※2 のれん以外にPurchase Price Allocationにより認識された無形固定資産の22/3期末残高は84百万円。これらの残存償却期間は5~9年。
※3 のれん以外にPurchase Price Allocationにより認識された無形固定資産の22/3期末残高は46百万円。これらの残存償却期間は5年。
※4 2022年3月期末の為替レートで換算した数値。
(3)受注残高の推移
|
22/3期 期末 (A) |
23/3期 第2四半期末 |
22年11月14日時点 (B) |
前期末比 (B-A)/A |
|
|
中外製薬 |
3,786 |
3,045 |
2,875 |
-24.1% |
|
エーザイ |
2,795 |
1,833 |
1,727 |
-38.2% |
|
その他 |
15,932 |
16,747 |
18,998 |
+19.2% |
|
受注残高合計 |
22,514 |
21,625 |
23,601 |
+4.8% |
*単位:百万円
同社のCRO事業において受託する治験業務では、1年から3年程度の治験実施期間において、症例数や対象疾患に起因する治験の難易度などにより受託総額が決定する。この実施期間についてクライアントと委受託契約を締結し、契約に従い売上が発生する。育薬事業においても、同程度の期間についてクライアントと委受託契約を締結し、契約に従い売上が発生する。
受注残高は、既に契約を締結済みの受託業務の受注金額の残高である。これは、今後1年から5年程度の期間で発生する売上高を示しており、同社グループの今後の業績予想の根拠となる指標である。
2022年11月14日時点の受注残高は、2022年3月期末と比較して4.8%増の236億1百万円と引き続き200億円を超え高水準となっている。
米国は、良好な取引関係にある米国バイオテック企業等からの大型の新規案件の受注や契約変更等により受注残高が増加した。また、現在、受注内定を受け契約締結交渉中の上記受注残高には含まれない案件がある他、これら以外にも新規案件の引き合いが増加している。
欧州は、治験計画の見直しによる契約変更により来期以降の売上となる予定であった受注残高の減少などもあったものの、複数の新規案件や期間延長等の契約変更により今期及び来期以降の売上に貢献する受注を獲得している。また、複数の新規案件の打診を受けており、受注の積み上げに向け、営業活動を継続している。
日本・アジアは、外資系製薬会社との間で新規の大型案件の契約があったことに加え、複数の新規案件の獲得や契約変更により受注残高が増加しており、新規案件の引き合いも増加傾向にある。
なお、現在受注の内定を受け契約締結交渉中の案件を含めると、実質的な受注残高は250億円を超える水準となっている。
(4)第2四半期(7-9月)の業績推移
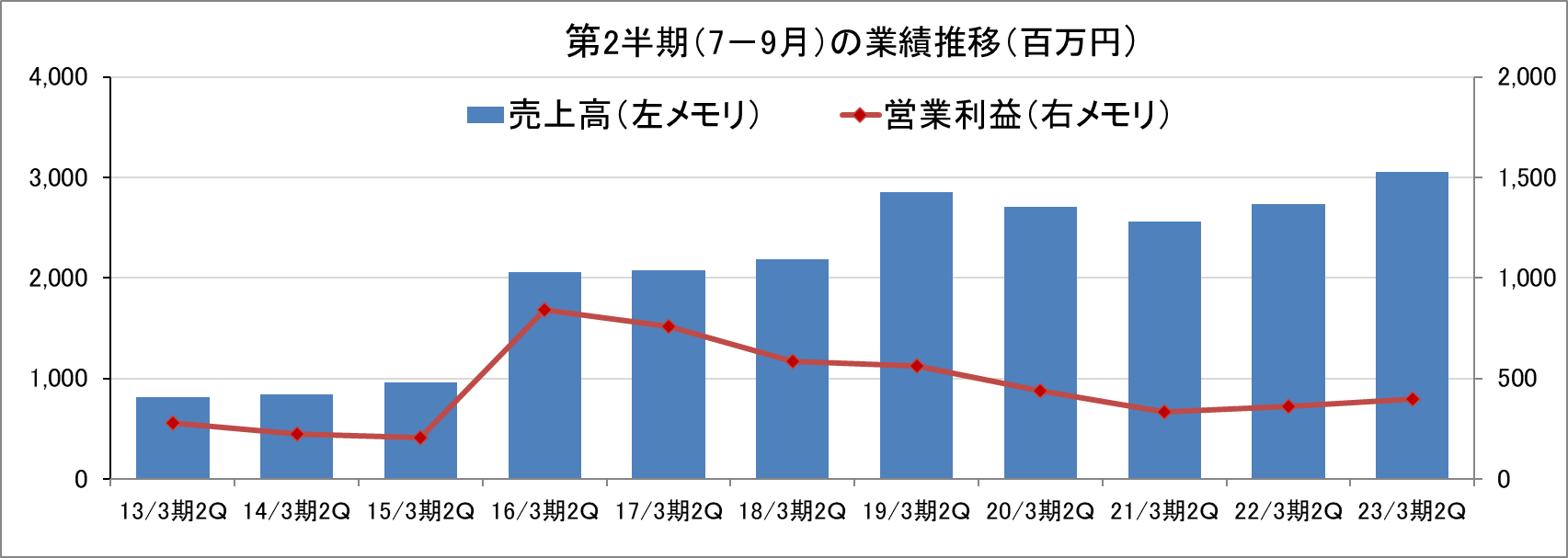
23/3期第2四半期(7-9月)は、前年同期比で増収増益となった。また、前四半期(4-6月)との比較においても増収増益となった。第1四半期の営業損失は、ロシア・ウクライナ戦争等の影響による欧米の大型国際共同試験の開始遅れなどにより稼働率が一時的に低下したことによるものであったが、第2四半期は米欧ともに挽回した。
(5)財政状態及びキャッシュ・フロー(CF)
財政状態
|
22年3月 |
22年9月 |
22年3月 |
22年9月 |
||
|
現預金 |
5,985 |
6,303 |
短期有利子負債 |
1,139 |
1,139 |
|
売上債権・契約資産 |
2,917 |
3,113 |
未払金・未払費用 |
936 |
1,133 |
|
立替金 |
987 |
1,438 |
前受金 |
2,147 |
2,411 |
|
流動資産 |
10,321 |
11,485 |
長期有利子負債 |
2,964 |
2,694 |
|
有形固定資産 |
664 |
664 |
負債 |
9,173 |
10,095 |
|
無形固定資産 |
3,565 |
3,916 |
純資産 |
6,543 |
7,170 |
|
投資その他 |
1,165 |
1,199 |
負債・純資産合計 |
15,716 |
17,265 |
|
固定資産 |
5,395 |
5,780 |
有利子負債合計 |
4,103 |
3,834 |
*単位:百万円
*有利子負債=借入金+リース債務
2022年9月末の総資産は前期末比15億49百万円増の172億65百万円。資産サイドは主に現預金、立替金、のれんなどが増加要因となり、投資有価証券などが減少要因となった。負債純資産サイドは、主に未払金、前受金、預り金、為替換算調整勘定などが増加要因となり、未払費用、長期借入金などが減少要因となった。2022年9月末ののれんは、37億65百万円となり、過去の欧米子会社買収時ののれんは外貨建てでは償却が進み減少するものの、円安の影響により円換算額での比較では前期末比3億58百万円増加した。また、2022年9月末の自己資本比率は41.5%と前期末から0.1ポイント低下した。
| キャッシュ・フロー | ||||
|
22/3期 第2四半期 |
23/3期 第2四半期 |
前年同期比 |
||
| 営業キャッシュ・フロー(A) |
836 |
659 |
-176 |
-21.2% |
| 投資キャッシュ・フロー(B) |
-31 |
-27 |
+4 |
– |
| フリー・キャッシュ・フロー(A+B) |
804 |
631 |
-172 |
-21.4% |
| 財務キャッシュ・フロー |
-821 |
-636 |
+185 |
– |
| 現金及び現金同等物期末残高 |
5,062 |
6,303 |
+1,240 |
+24.5% |
*単位:百万円
CF面では、為替差益の拡大、立替金の増加などにより、営業CFのプラス幅が縮小した。また、投資有価証券の取得による支出の減少などにより投資CFのマイナス幅が縮小したものの、フリーCFのプラス幅も縮小した。一方、長期借入金の返済の減少などにより財務CFのマイナス幅が縮小した。これらにより、期末のキャッシュポジションは、前期末比で24.5%増加した。
(6)新市場区分の上場維持基準の適合に向けた計画書
同社は、2022年4月よりプライム市場の上場となった。一方、移行基準日時点(2021年6月30日)で、流通株式時価総額において当該市場の上場維持基準を充たしていないことから、上場維持基準の適合に向けた計画書を作成した。
具体的には、2023年3月期~2025年3月期の3か年で、中期経営計画に基づき (1) 収益力の強化、(2) コーポレートガバナンスの強化、(3) アカウンタビリティの強化を通じて、流通株式時価総額の増加を図る方針である。
【具体的な取組内容】
|
(1)収益力の強化 |
|
| ターゲットとする顧客層の拡大 | 従来の日系大手製薬会社を中心とした顧客層を、海外大手製薬会社、国内外の
バイオテックカンパニーまで拡大 |
| ターゲットとする疾患領域の拡大 | 再生医療、細胞医薬、核酸医薬、治療アプリなど最新のモダリティを活用した治療法に対応することで、従来のがん・中枢・免疫領域を中心としたサービス提供から、
眼科、皮膚科、希少疾患等まで拡大 |
| サービス領域の拡大 | 国内外の顧客に対する、市場分析、開発戦略策定、当局対応等のクライアントニーズにマッチしたコンサルティングサービスの強化により競合他社と差別化 |
| 海外事業の拡大 | 巨大医薬品市場である米国・欧州を重点戦略エリアとして営業を強化するとともに、
将来の更なるM&Aも視野に、海外事業の基盤強化・拡大を促進 |
| 財務基盤の強化 | 米国、欧州での更なるM&A等の大型成長投資に備え、有利子負債の圧縮を進め、
自己資本比率の改善を促進するとともに、自己株式の売却等による財務基盤の強化と成長投資資金の確保を検討 |
|
(2)コーポレートガバナンスの強化 |
|
| 経営の透明性・健全性の向上 | 経営の透明性・健全性をより一層向上させるため、取締役に占める独立社外取締役比率の増加及び監査等委員会設置会社への移行等を積極的に検討 |
| 人材の戦略的多様化 | 女性、中途採用者、外国人など従業員の多様性を確保し、会社の持続的な成長に資する中核人材を育成するとともに、公平かつ生産性の向上につながる人事評価制度など人事関連諸制度について継続的に改善 |
|
(3)アカウンタビリティの強化 |
|
| 情報開示の充実 | 中長期的な企業価値の向上のため、情報開示の充実を継続的に推進するとともに、招集通知・その他の開示書類の英文化を推進 |
| 投資家との対話の推進 | 従来の機関投資家・アナリスト・個人投資家向けの決算説明会に加え、国内外の機関投資家との個別ミーティング等の対話機会をこれまで以上に促進 |
【中期目標】
|
2021/3期 実績 |
2022/3期 実績 |
2023/3期 中計 |
2024/3期 中計 |
2025/3期 中計 |
|
|
売上高 |
10,279 |
11,555 |
11,420 |
12,086 |
12,814 |
|
営業利益 |
453 |
1,085 |
658 |
880 |
1,001 |
*単位:百万円
同社は、上場維持基準の適合に向けた計画書の中で示した中計の目標である2023/3期の売上と2025/3期の営業利益を2022/3期に前倒して達成した。今後中計を見直し、持続的な成長と収益力の向上による中長期での企業価値向上を目指す方針である。
4.2023年3月期業績予想
(1)連結業績
|
22/3期 実績 |
構成比 |
23/3期 予想 |
構成比 |
前期比 |
|
|
売上高 |
11,555 |
100.0% |
12,440 |
100.0% |
+7.7% |
|
営業利益 |
1,085 |
9.4% |
1,224 |
9.8% |
+12.7% |
|
経常利益 |
1,183 |
10.2% |
1,204 |
9.7% |
+1.7% |
|
親会社に帰属する 当期純利益 |
790 |
6.8% |
871 |
7.0% |
+10.2% |
*単位:百万円
前期比7.7%の増収、同12.7%の営業増益
第2四半期が終わり、23/3期の会社計画は、売上高が前期比7.7%増の124億40百万円、営業利益が同12.7%増の12億24百万円の予想から修正なし。受注案件の進捗管理の徹底による売上計上の迅速化と内定案件の早期契約締結・業務開始、及び、現在交渉中の新規案件獲得による売上の積み増しに取り組むとともに、受注案件に応じた人件費、経費の厳密なコントロールを実施することにより、通期の会社計画の達成を目指す。
売上高は、欧米事業において順調に大型グローバル案件の受注獲得が進んでいることから前期比で増加する。また、営業利益も欧米での事業拡大に伴う人材投資や、業務のデジタル化や情報セキュリティ等のIT投資が発生するものの、日本事業を中心に売上原価を厳密にコントロールすることで、前期比増加する見込みである。
売上高営業利益率は、前期比0.4ポイント上昇の9.8%の見込み。経常利益は、為替差益を見込まず前期比1.7%増益と営業利益の増益率を下回る計画となっている。
また、配当も前期と同額の1株当たり普通配当14円の予定を据え置き。同社は、内部留保を、従業員の雇用や海外拠点設立などの成長原資として活用し、中長期的な企業価値の向上を目指しており、当面安定的な利益還元を実施する方針である。
(2)中期の経営ビジョン
同社は、To be the “strongest” CROを標榜し、最大ではなく、最強のCROを目指している。 最強のCROになるためには、労働集約的ではなく知識集約的であり、業界で最高の収益性を達成する必要がある。これを達成するため、チームの各メンバーは、一人当たりの収益の点で競合他社をしのぐことを目指している。
また、同社の中期経営ビジョンは、「日本発のグローバルCROとして、クライアントの戦略的パートナーに」であり、今後以下の戦略を集中して実施する。
| Business Focus | ◆臨床試験に関わるサービスをグローバル・ワンストップで提供する。
◆臨床試験の全てのフェーズを対象とする。 ◆がん・中枢系など開発難易度の高い疾患を中心とした高品質・スピーディなサービスを提供する。 |
| Client Focus | ◆大手製薬企業から欧米の有望なバイオテックカンパニーまで幅広いクライアントと長期的かつ戦略的なパートナー関係を構築する。
◆品質にコミットするとともに、スピード感をもって柔軟にサービスを提供し、クライアント満足を追求 する。 |
| Global Coverage | ◆主要なマーケット(日本、米国、欧州)を中心に幅広い国と地域をカバーする。
◆南半球を含め戦略的にサービス提供エリアを拡大し、あらゆる疾患のデータを迅速に収集できる体制とすることでグローバルでのプレゼンスを高めていく。 |
更なるエリア拡大の可能性
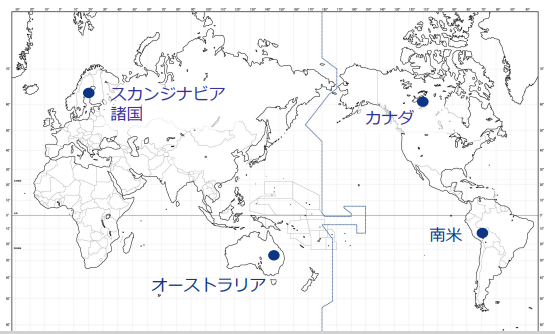
5.今後の注目点
同社の22/3期第2四半期決算は、前年同期比7.2%の増収ながらも、同26.4%の営業減益となった。残念ながら営業利益は前年同期比で減益となったものの、四半期ベースでは大幅な改善が図られた。第1四半期(4-6月)は26百万円の営業損失となったものの、第2四半期(7-9月)は4億円の営業利益となった。第1四半期はロシア・ウクライナ戦争等の影響による欧米の大型国際共同試験の開始遅れなどにより稼働率が一時的に低下したものの、第2四半期は米欧ともに挽回したものである。上期の営業利益は通期の会社計画の営業利益に対して30%程度の進捗と通期の会社計画の達成が困難に見える。しかし、下期の会社計画の営業利益は8億51百万円であり、第2四半期(7-9月)の営業利益が4億円程度まで収益力が高まっていることを考えると下期の会社計画の達成が困難とは言えない。同社は、下期において受注案件の進捗管理の徹底による売上計上の迅速化と内定案件の早期契約締結・業務開始、及び、現在交渉中の新規案件獲得による売上の積み増しに取り組むとともに、受注案件に応じた人件費、経費の厳密なコントロールを実施することにより、通期の会社計画の達成を目指す。通期の会社計画の達成に向けてどこまで利益を積み上げることができるのか、続く第3四半期の業績動向が注目される。加えて、同社は中計において目標としていた23/3期の売上高と25/3期の営業利益を22/3期に前倒して達成しており、今後中計の業績目標の上方修正が実施される可能性が高い。どのような中計の業績目標となるのか注目される。
また、足元好調な受注環境が継続している。2022年11月14日時点の受注残高は、2022年3月期末と比較して4.8%増の236億1百万円と引き続き200億円を超え高水準となっている。加えて、現在受注の内定を受け契約締結交渉中の案件を含めると、実質的な受注残高は250億円を超える水準となっている模様である。今後の業績拡大の先行指標となる受注残高をどれ位の水準まで積み上げることができるのか注目される。
更に、リアルワールドデータの医薬品開発への利活用の活発化は、今後同社へ大きなビジネスチャンスをもたらすものと期待される。中長期的な話とはなるものの、グローバルなリアルワールドデータの活用が同社のCRO事業並びに育薬事業にどのような恩恵をもたらすのについても期待を込めて注目したい。
<参考:コーポレート・ガバナンスについて>
◎組織形態および取締役・監査役の構成
| 組織形態 | 監査役設置会社 |
| 取締役 | 9名、うち社外2名 |
| 監査役 | 3名、全員社外監査役 |
◎コーポレート・ガバナンス報告書
最終更新日:2022年6月30日
<基本的な考え方>
(1)経営理念
当社は、「医薬品開発のあらゆる場面で常にプロフェッショナルとしての質を提供し、ステークホルダーである製薬会社、医療機関、患者ならびに株主、従業員の幸せを追求する。」を経営理念として掲げています。役員・従業員の有する知識・経験、
組織としてのノウハウ・システムを持続的に発展・維持し、製薬会社など世界中のヘルスケアカンパニーに提供することで、
新薬を含む新しい治療技術の開発やその発展・浸透、ひいては人類の健康的な生活に貢献することを目指しています。
(2)コーポレート・ガバナンスに関する基本的な考え方
上記経営理念に基づき、当社は、医薬品開発のノウハウ・技術をもって新薬を含む新しい疾患予防・治療技術の誕生・成長に貢献し、国内外のバイオベンチャー、製薬企業、医療機器メーカーなどのヘルスケアカンパニー、医療機関のパートナーとして医療の発展に貢献し、患者様ならびに社会全体の期待に応えてまいります。
当社は、人命に関わる事業活動を行うため、当社の役員ならびに従業員には専門性のみならず高い倫理観が求められることから、コンプライアンスの徹底をはじめとした企業行動規範の遵守を徹底しております。また、内部統制の充実を図り、経営の健全性・透明性を確保することで、事業の発展とあわせて企業価値の向上に努めております。
<コーポレート・ガバナンス・コード各原則の実施について>
実施をしないコードのおもな原則と理由
|
原則 |
実施しない理由 |
| 【補充原則1-2④ 株主総会における権利
行使】 |
当社は、株主が議決権行使を行いやすい環境の整備は必要であると認識しております。議決権の電子行使を可能とするための環境作り(議決権電子行使プラットフォームの利用等)については、機関投資家並びに海外投資家の比率等を勘案しながら、導入を検討してまいります。 なお、招集通知の英訳は当社Webサイトに掲載しています。
URL: https://www.linical.co.jp/en/news/17thOrdinaryGeneralMeetingofShareholders.pdf |
| 【原則1-3 資本政策の基本的な方針】 | 当社は、株主価値を中長期的に高め、持続的成長を実現するため、財務健全性の確保と持続的成長に向けた戦略的投資を行います。
具体的には、財務健全性の確保については、成長投資とリスクを許容できる株主資本の水準を保持することを基本とします。持続的成長に向けた戦略的投資については、内部留保資金を、将来の事業発展に必要不可欠な国際共同治験への体制構築のための投資やM&Aによる拠点拡充などに活用し、資本効率の向上に努めます。 株主への利益還元である配当については、中長期的な成長による企業価値向上と利益還元のバランスの最適化を図ることを基本方針とし、安定的な利益還元に努めます。以上の資本政策の基本的な方針に関し、今後、Webサイト上等でご説明できるよう検討してまいります。 |
| 【補充原則2-4① 中核人材の登用等における多様性の確保】 | 当社では、多様性の確保の自主的かつ測定可能な目標を現時点において定めておりませんが、【コーポレートガバナンス・コードの各原則に基づく開示】の補充原則2-4①に係る記載のとおり、当社グループでは、女性、中途採用者等の多様性確保は一定程度進んでいるものと判断しております。今後も多様な人材の活躍を推進し、従業員一人ひとりがそれぞれの能力・特性を最大限に発揮できるよう環境の整備や人材の育成を継続的に行ってまいります。 |
| 【補充原則3-1③ サステナビリティについての取組み等】
【補充原則4-2② 自社のサステナビリティを巡る取組みについての基本方針の策定等】 |
1.サステナビリティへの取り組み
当社は「医薬品開発のあらゆる場面で常にプロフェッショナルとしての質を提供し、ステークホルダーである製薬会社、医療機関、患者ならびに株主、従業員の幸せを追求する。」という経営理念に基づき、社会と共に持続可能な発展を目指しています。この実現に向け、「革新的な医薬品の開発支援」及び「医薬品の安全性の確保」の2つの使命を常に念頭に事業を行っています。具体的には、臨床試験に携わる企業として、被験者をはじめとした関係するすべての人の人権・個人の尊厳の尊重を原則とした企業行動規範を定め、これを遵守することで役員・従業員一人ひとりが「社会的責任」を意識し、誠実さをもって企業活動を遂行しています。また、設立以来、難易度の高くアンメットメディカルニーズの多い領域の医薬品開発に率先して取り組む方針を掲げており、事業活動を通じて世界中の人々の健康で豊かな生活に貢献すること追求しています。 以上の考え方に基づき、サステナビリティをめぐる取組みについての基本方針、情報開示の枠組みや具体的な重要課題について、現在検討しております。 2.人的資本への投資 医薬品開発のプロフェッショナルとして様々なサービスを提供する当社にとって、社員こそが価値創造の源泉であると考えています。補充原則2-4①に記載した通り、従業員一人ひとりがそれぞれの能力・特性を最大限に発揮できるための環境の整備や、薬学的知識をはじめとした必要な知識や技能の獲得のための教育研修プログラムを充実させています。 また、グローバルに事業を拡大しており、国際共同治験も増加している環境下で、多様な文化的背景を持つ人々とコミュニケーションができる人材の育成にも注力しており、その前提となる英語研修の強化および異文化理解研修を定期的に行っています。さらには、海外子会社(欧米、中国など)での若手の駐在の機会も提供しグローバル人材の育成に取り組んでいます。 3.気候変動 当社はその重要性・緊急性を認識し、関連部門によるワーキングチームにおいて気候変動に関するデータの収集と分析を実施し、GHG排出量としてScope2についての実績を以下に開示します(Scope1は該当なし)。今後、TCFD(気候関連財務情報開示タスクフォース)の枠組みに沿った情報開示の充実を進めます。現時点の検討状況は以下の通りです。 ・ ガバナンス 取締役会は気候変動に関する報告を受けています。今後、気候変動に対するガバナンスを強化していくための体制について検討していきます。 ・ 戦略 当社における気候変動に関する重要なリスクと機会については今後、具体的な対応策とともに検討を進めます。 ・ リスク管理 気候変動リスクの全社的リスク管理への統合プロセスについては検討中であり、今後開示を進めていきます。 ・ 指標と目標 気候変動の評価指標、目標に関しては今後検討していきます。GHG排出量(Scope2)の実績は下記のとおりです。 GHG排出量(Scope2) 2021年 2020年 単体(日本) 290.5t-CO2 289.7t-CO2 連結(グローバル) 345.9t-CO2 341.0t-CO2 ※Scope1に該当する排出はなし。Scope2は外部から購入した電力。 ※排出係数は、国内は電力会社別の調整後排出係数、海外はIEA最新のデータ (2021edition)による CO2 換算係数を使用 |
| 【補充原則4-10① 独立した指名委員会・報酬委員会の設置による独立社外
取締役の適切な関与・助言】 |
当社は、独立社外取締役は現在2名であり、各取締役、経営陣との連絡・調整、監査役との連携体制は構築されており、取締役会において、指名・報酬などについても十分な議論を行い、コーポレートガバナンス・コードの趣旨にのっとった実効性の高い審議・監督は出来ていると考えております。 |
<開示している主な原則>
|
原則 |
開示内容 |
| 【補充原則2-4① 中核人材の登用等における多様性の確保】 | 1 多様性確保についての考え方
当社グループは、世界の医薬品開発に貢献できるグローバル企業として成長するため、変化し続ける社会や多様な価値観に柔軟に対応すべく多様な人材の活躍を推進し、従業員一人ひとりがそれぞれの能力・特性を最大限に発揮できるよう環境の整備や人材の育成を行っています。 2 中核人材の多様性推進に関する状況 (1)女性 日本本社およびグループ全体で女性管理職の登用は進んでおり、今後、経営の中核を担う執行役員以上の女性リーダー育成に向け、さらなる環境の整備やキャリア形成支援を行ってまいります。 【本社(日本)】 2022年3月末 2021年3月末 女性社員比率 61.6% 44.4% 女性管理職比率 42.6% 19.4% 女性執行役員比率 16.7% 16.7% 【グループ】 女性社員比率 67.5% 58.6% 女性管理職比率 56.9% 36.5% 女性執行役員比率 28.6% 25.0% (2)外国人 当社グループ従業員843名(2022年3月末時点)の約50%が海外に居住する現地採用の社員であり、海外グループ会社においてはCEOをはじめとした主要なポジションのほとんどを現地の優秀な人材が担っています。また、日本本社においても国籍を問わない人材採用を進めています。 2022年3月末時点の日本本社の全社員に占める外国籍社員比率は6.7%、管理職の外国籍社員比率は3.0%です。 (3)中途採用者 2022年3月末時点の日本本社の全社員に占める中途採用者比率は41.5%です。また、執行役員の中途採用者比率は100%、管理職の中途採用者比率は76.2%です。グループ全体では、2022年3月末時点の全社員に占める中途採用者比率は66.9%であります。また、執行役員の中途採用者比率は100%、管理職の中途採用者比率は85.1%です。 3 多様性の確保に向けた人材育成方針、社内環境整備方針、その状況 当社グループは、従業員個々の特性や能力を最大限発揮させるための施策として、多様なライフイベントを経ても仕事と生活のバランスを図りつつ働きやすい環境の整備を進め、週休3日制勤務やフレックスタイム勤務、リモートワーク勤務、短時間勤務制度等、国ごとに働きやすい制度を策定し、運用しています。 また、人権の尊重やハラスメント禁止等の規定を含む、各種ポリシー・手順書について、グローバル共通の共有・学習システムを導入し、遵守徹底を図っています。 |
| 【原則3-1 情報開示の充実】 | (i)会社の目指すところ(経営理念等)や経営戦略、経営計画
当社は、「医薬品開発のあらゆる場面で常にプロフェッショナルとしての質を提供し、ステークホルダーである製薬会社、医療機関、患者ならびに株主、従業員の幸せを追求する。」を経営理念として掲げ、持続的な成長と中長期的な企業価値向上を目指しています。この実現に向け、2025年3月期を最終年度とする3か年の中期経営計画を策定しており、プライム市場上場維持基準の適合に向けた計画書において公表しています。経営戦略、経営計画の詳細につきましては、有価証券報告書などの資料にて開示していますので、当社WEBサイトをご参照ください。 URL: (ii)本コードのそれぞれの原則を踏まえた、コーポレートガバナンスに関する基本的な考え方と基本方針 コーポレート・ガバナンスに関する基本的な考え方については、本報告書の「Ⅰ.基本的な考え方」に記載しています。またこれを含めた当社コーポレート・ガバナンスの概要については当社WEBサイトにて開示しています。 URL: https://www.linical.co.jp/ir/corporate_governance.html
(iii)取締役会が経営陣幹部・取締役の報酬を決定するに当たっての方針と手続 当社は、2021年5月31日開催の取締役会において、取締役の個人別の報酬等の内容に係る決定方針を決議しております。取締役の個人別の報酬等の内容に係る決定方針 イ.取締役報酬の基本方針 当社の取締役報酬制度は、経営理念に基づく当社グループの持続的な成長と中長期的な企業価値の向上を実現し、また、業務執行・経営監督等の機能が、透明性・公平性を保ちつつ適切に発揮されることを目的として定めております。当社の取締役報酬制度の基本的な考え方は以下のとおりです。 a.報酬等の種類ごとの割合の決定方針 取締役の報酬等の種類は、固定の金銭報酬である基本報酬のみとします。現在、当社の業務執行を担う取締役は、会社の設立メンバーであり、既に一定数の当社株式を保有しております。そのため、単年度及び中長期の業績を反映した株主価値の増減が保有株式の価値の増減と連動しており、実質的な業績連動報酬を内包しているものと考えております。このような観点から、現時点において業績連動賞与や株式報酬等の非金銭報酬を設定しておりません。なお、今後の設立メンバー以外の業務執行を担う取締役の就任など会社組織形態の変化に応じて役員報酬制度についても必要な変更を検討してまいります。 b.報酬等(業績に連動しない金銭報酬)の額またはその算定方法の決定方針 取締役の報酬については、株主総会で決議した報酬等の総額(注)の範囲内において、取締役会で経済情勢、会社業績や経営内容、役員構成などを総合的に勘案し、報酬総額を年度予算として確定します。 取締役の報酬は取締役が職務に専念できるように固定の金銭報酬である基本報酬(月例定額報酬)とし、各取締役の役位、職責の内容に応じた基本部分と、職責のリスクに応じたリスク手当部分、並びに在任年数に応じた功績部分の3つから構成されます。 (注)取締役の報酬限度額は、2007年6月27日開催の第2回定時株主総会において年額800百万円以内(ただし、使用人分給与は含まない。 定款で定める取締役の員数は13名以内で、本有価証券報告書提出日現在は9名。)と決議いただいており、また、監査役の報酬限度額は、2007年6月27日開催の第2回定時株主総会において年額200百万円以内(定款に定める監査役の員数は4名以内で、本有価証券報告書提出日現在は3名)と決議いただいております。 ロ.個人別の報酬等の決定に関する方針 各取締役に支給する基本報酬については、取締役会決議に基づき代表取締役社長にその具体的内容の決定を委任するものとし、代表取締役社長は、当社の業績等も踏まえ、取締役会で決議した報酬総額の範囲内において、各取締役の役位、職責等に応じて決定します。 ハ.取締役に対し報酬等を与える時期等 基本報酬は、月例の定額報酬とします。 (iv)取締役会が経営陣幹部の選解任と取締役・監査役候補の指名を行うに当たっての方針と手続当社では、取締役および執行役員候補については、法令及び企業倫理の遵守に徹する見識を有すること、的確かつ迅速な意思決定が行えること、そのほか個人の知識・経験・能力等に基づき、経営陣・取締役会全体のバランスを総合的に考慮した上、選任・解任・指名することとしています。この方針に基づき、代表取締役が独立社外役員の助言を得ながら候補者を推薦し、経営会議、取締役会で議論を経て決定します。監査役候補については、個人が持つ財務・会計、企業経営、及び当社事業に関する知識や多様な視点を鑑み、適切に経営の監視活動が行える環境を整えるべく総合的に判断しており、この方針に基づき、監査役会が提案あるいは同意を決議し、取締役会で決定します。 (v)取締役会が上記(iv)を踏まえて経営陣幹部の選解任と取締役・監査役候補の指名を行う際の、個々の選解任・指名についての説明取締役候補・監査役候補の選任・解任・指名につきましては、株主総会招集通知に個人別の経歴、候補者とした理由を記載しております。 当社WEBサイトをご参照ください。 URL: https://ssl4.eir-parts.net/doc/2183/ir_material4/185146/00.pdf
|
| 【原則5−1 株主との建設的な対話に関する方針】 | 当社は、株主(潜在株主としての機関投資家や個人投資家を含む)との建設的な対話を通じて、企業と株主との共通目的である企業価値の持続的成長を目指しています。プライム市場の選択に伴い開示している「上場維持基準の適合に向けた計画書」において、アカウンタビリティの強化を掲げており、情報開示の充実を継続的に推進し、国内外の投資家との対話の促進に取り組んでいます。具体的には、業績、経営戦略、資本政策、リスク、コーポレートガバナンス体制などについて以下の方法により継続的・建設的で透明・公正な対話を実施しています。
・ 株主との対話は専務取締役CFOが統括を行い、面談の目的と効果、株主属性を勘案し、代表取締役社長、専務取締役CFOを中心とした経営幹部により対話者と対話方法を検討のうえ実施しています。 ・ IRは財務部ならびに広報室が中心となり社内関連部署から必要情報を収集し、分かり易い資料作成や説明により株主との対話を充実させています。 ・ 定時株主総会、決算説明会、個人投資家向け説明会に加え、国内外機関投資家との個別ミーティング、英文を含めたWebサイトでのIR情報開示、個人投資家様からの電話・メール等による個別対応などを通じて対話の機会を持ち、質問や要望、説明会での参加者情報やアンケート結果などをIR活動へ反映しています。 ・ 株主との対話を通じて把握した株主の関心や懸念は専務取締役CFOに集約し、経営分析や情報開示の在り方などの検討に活かしています。 ・ IR活動や株主との対話においては、社内規程の定めるところに従い、適切にインサイダー情報を管理しております。なお、当社では決算情報に関する対話を控える沈黙期間を四半期決算期日の翌日から決算短信発表日までを沈黙期間としております。 |

